В декабре 2019 г. в самом густонаселенном городе центрального Китая была зарегистрирована вспышка пневмонии, вызванная ранее неизвестным видом коронавируса, которому было присвоено официальное таксономическое наименование SARS-CoV-2. Коронавирус SARS-CoV-2, наряду с вирусом SARS-CoV, относится к семейству Coronaviridae, подсемейству Orthocoronavirinae, роду Betacoronavirus, подроду Sarbecovirus, виду Severe acute respiratory syndrome-related coronavirus [1–2]. В течение короткого времени вирус из Китая распространился по странам и континентам, в начале марта ВОЗ объявила о пандемии инфекции, получившей название COVID-19. К настоящему времени в мире было зарегистрировано более 616,5 млн случаев заболевания, из которых более 6,5 млн закончились смертельными исходами.
Характер заболевания, вызванного SARS-CoV-2, может различаться у разных людей в широких пределах [3]. В клинической практике наблюдается большая вариабельность клинических проявлений COVID-19 даже среди близких контактов инфицированного и членов одной семьи. Спектр симптоматики при COVID-19 колеблется от легкой и умеренной формы до критической и фатальной [4–6]. Также часто фиксируются случаи бессимптомного течения заболевания. Кроме того, бессимптомное течение инфекции может быть ассоциировано с субклиническими нарушениями в легких, которые выявляются при проведении компьютерной томографии [7]. Таким образом, SARS-CoV-2 обладает повышенной вирулентностью с тактическим преимуществом – способностью поддерживать передачу от человека человеку даже при бессимптомном носительстве [8], что позволяет вирусу быстро распространяться. Заболевание COVID-19 в тяжелой форме может протекать у практически здоровых людей любого возраста, но преимущественно встречается у лиц старше 65 лет и/или в группах риска – у людей с сопутствующими заболеваниями (сердечно-сосудистые заболевания, сахарный диабет, гипертония, хронические заболевания легких и почек, онкологические заболевания, ожирение, курение) [5, 9, 10]. В настоящее время вакцинация против коронавирусной инфекции рассматривается как основное средство профилактики заболевания и способ остановить пандемию. За очень короткое время в мире созданы и зарегистрированы несколько вакцин против коронавирусной инфекции. Однако известно, что ни одна вакцина не обладает 100% эффективностью. Кроме того, изменчивость нового коронавируса оказалась значительно выше, чем ожидалось, постоянно возникают новые варианты вируса, в отношении которых эффективность существующих вакцин снижена. Поэтому другим направлением борьбы с коронавирусной инфекций является применение лекарственных препаратов. Несмотря на определенные успехи в этой области вопрос о медикаментозной терапии COVID-19 остается открытым. Создание новых специфических препаратов для лечения новой инфекции является длительным процессом, занимающим при наилучшем стечении обстоятельств несколько лет. С целью сдерживания распространения вируса и создания резерва необходимых лекарственных препаратов все медицинское сообщество фокусируется на использовании уже существующих зарегистрированных препаратов, обладающих эффективностью в отношении других инфекций [11, 12]. При этом проведение полноценных клинических испытаний было невозможно в условиях геометрически усиливающей волны заболеваемости в начале и середине пандемии и затруднено в настоящее время. В связи с этим экспериментальное изучение активности уже апробированных препаратов может определить их эффективность в отношении новой инфекции, Часто оно являлось одним из оснований для начала применения таких препаратов в клинической практике и включения их в рекомендации по лечению COVID-19.
Мирамистин® [бензилдиметил 3-(миристоиламино) пропиламмония хлорида моногидрат – БМПА] – оригинальный лекарственный препарат из группы катионных поверхностно-активных веществ. Многочисленными экспериментальными исследованиями подтверждено, что он обладает выраженным антимикробным действием в отношении грамположительных и грамотрицательных бактерий, грибов, вирусов, простейших, аэробной, анаэробной флоры, находящейся в виде монокультур и микробных ассоциаций, включая штаммы, полирезистентные к лекарственным препаратам. Препарат имеет низкую токсичность, не обладает местнораздражающим, аллергизирующим, мутагенным, канцерогенным и эмбриотоксическим действием. Его вирулицидные свойства исследованы по отношению к лабораторным штаммам вирусов гриппа (H3N2), гепатита, аденовирусов, герпесвирусов I и II типа, коронавируса ОС43, ECHO 6-го типа, полиовирусов 2-го типа, Коксаки В1 и В6, колифага Т2, а также вирусу иммунодефицита человека (ВИЧ) [13–17].
Целью работы явилось изучение и лабораторное подтверждение влияния оригинального лекарственного препарата БМПА на инфекционную активность коронавируса SARS-CoV-2 in vitro.
Исследование выполнено с использованием оборудования Центра коллективного пользования НИИВС им. И.И. Мечникова
Материалы и методы
Образцы и их приготовление
Образец активной фармацевтической субстанции БМПА (бензилдиметил-миристоиламино-пропиламмоний) был предоставлен ООО «ИНФАМЕД» (Россия). Субстанцию в форме порошка растворяли в поддерживающей среде до концентрации 0.64% (сток-раствор) и далее разводили до необходимых концентраций с использованием поддерживающей среды (среда DМЕМ на основе буфера Эрла с добавлением 300 мкг/мл L-глутамина, 40 мкг/мл гентамицина («ПанЭко», Россия).
Вирус и культура клеток
В работе использовали лабораторный штамм коронавируса SARS-CoV-2: Dubrovka (идент. № GenBank: MW514307.1, классификация по Pango B.1.1.317, филогенетически близкий к штамму Wuhan-Hu-1, идент. № GenBank: MN908947.3). Штамм был выделен на культуре клеток Vero CCL81 из назофарингеального мазка больного с подтвержденным диагнозом COVID-19, прошел 20 последовательных пассажей и вызывал выраженное цитопатическое действие (ЦПД) [18]. Культивирование вируса проводили на клетках эпителия почки африканской зеленой мартышки Vero CCL81 (ATСС) из коллекции НИИВС им. И.И. Мечникова при 37 ⁰С в питательной среде DМЕМ с L-глутамином (300 мкг/мл) и глюкозой 4,5 г/л, смесью антибиотиков (пенициллин 100 МЕ/мл и стрептомицин 100 мкг/мл) в атмосфере 5% СО2. Образцы вирусного материала для проведения работы хранились при температуре -80 ⁰С в виде аликвот. Для титрования вирусного материала и характеристики вируса использовали перевиваемую культуру клеток эпителия почки африканской зеленой мартышки Vero CCL81.
Определение титра вируса
Титр вируса SARS-CoV-2 определяли по конечной точке проявления ЦПД в культуре клеток Vero. Клетки рассаживали в 96-луночных планшетах фирмы Costar со средней плотностью 10 000 клеток на лунку и выращивали в среде DМЕМ в присутствии 5 % фетальной сыворотки телят, 10 мМ глутамина и антибиотиков (пенициллин 100 МЕ/мл и стрептомицин 100 мкг/мл) до формирования полного монослоя (в течение 3 дней). Перед заражением вирусом культуру клеток 2 раза промывали средой DМЕМ без сыворотки. Готовили 10-кратные разведения вируса и приготовленные разведения в объеме 200 мкл вносили в планшеты с культурой клеток и инкубировали в атмосфере 5% CO2 при 37 °С. Результаты титрования учитывали визуально путем микроскопического исследования клеточного монослоя на наличие характерного ЦПД на 5-е сутки после заражения (округление и открепление клеток от монослоя). Расчет титра вируса проводили с использованием формулы M.A. Ramakrishnan в программе Excel [19] и выражали в lg ТЦИД50/ мл (тканевой цитопатической инфекционной дозы 50).
Количественное определение РНК вируса SARS-CoV-2
Количественное определение РНК вируса SARS-CoV-2 проводили методом ОТ-ПЦР-РВ [20].
Оценка цитотоксичности препарата в МТТ- тесте с определением МПК и ЦТД50 в культуре клеток Vero
Из сток-раствора препарата готовили исследуемые разведения, которые вносили в клетки с последующей инкубацией в атмосфере 5% CO2 при 37 °С в течение 5 сут. В другой модификации определения цитотоксичности эти же разведения добавляли к клеткам и инкубировали в течение 60 мин. После этого препарат удаляли, к монослою клеток после двукратной отмывки добавляли поддерживающую среду и инкубировали в атмосфере 5% CO2 при 37 °С в течение 3 сут. В обоих модификациях по окончании срока инкубации проводили микроскопическое исследование монослоя клеток на наличие признаков токсичности. После этого в колориметрическом МТТ-тесте спектрофотометрически оценивали выживаемость клеток [18]. Для этого в лунки 96-луночного планшета с клетками добавляли по 20 мкл раствора МТТ (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide), 5 мг/мл («ПанЭко», Россия) и инкубировали при 37 °C в атмосфере 5% CO2 в течение 2 ч. Культуральную жидкость отбирали и добавляли в лунки по 100 мкл ДМСО (Sigma-Aldrich, кат. номер D4540-1L) в каждую лунку. С помощью планшетного спектрофотометра определяли оптическую плотность (ОП) каждой лунки при 530 нм с учетом фоновых значений при 620 нм.
Выживаемость клеток рассчитывали по формуле:
![]()
где ОП530 опытной пробы – среднее значение ОП530 в лунках с исследуемым препаратом;
ОП530 клеточного контроля – среднее значение ОП530 в лунках с клеточной культурой без препарата.
Максимальная концентрация препарата (МПК), не изменяющая значение ОП по сравнению с контролем клеток, принимается за МПК. Концентрация субстанций, уменьшающая значение ОП на 50% по сравнению с контролем клеток, принималась за ЦТД50, вычисление которой проводили в программе RStudio (Version 1.3.1093) на основе анализа четырехпараметрической логистической модели зависимости «доза–ответ».
Оценка вирулицидной активности БМПА
Диапазон разведений БМПА 0.04, 0,02 и 0,01% инкубировали в течение 30 мин. с культуральной средой без сыворотки, содержащей вирус SARS-CoV-2 в титре 105 ТЦИД50/ мл при 37 °С. После инкубации инфекционный титр проб определяли путем титрования вируса в культуре клеток Vero как описано выше. Из полученного материала готовили серии 10-кратных разведений (10-1–10-8) в поддерживающей среде. Их вносили в лунки 96-луночного планшета и инкубировали в атмосфере 5% CO2 при 37 °С в течение 5 сут. до появления выраженного ЦПД в клетках вирусного контроля. По окончании срока инкубации оценивали проявление вирусспецифического ЦПД в клетках микроскопически и с использованием МТТ-теста, как описано выше, и рассчитывали титр вируса.
В части опытов 3 наиболее эффективные концентрации БМПА 0,04, 0,02 и 0,01% инкубировали в течение 30 мин. с культуральной средой без сыворотки, содержащей вирус SARS-CoV-2 в титре 105 ТЦИД50/мл (104 ТЦИД50/100 мкл) при 37 °С. После инкубации смесь препарата и вируса разбавляли в пропорции 1:10 культуральной средой без сыворотки и вносили в лунки 24-луночного планшета с культурой клеток Vero в объеме 1 мл. Для снижения токсичности препаратов БМПА через 2 ч проводили замену смеси препарата с вирусом на поддерживающую среду без сыворотки в объеме 1 мл и инкубировали при 37 °С. Отбор среды проводили на 1-е и 2-е сутки после внесения смеси (30 мкл образца для определения титра вируса по ЦПД, а также 100 мкл культуральной жидкости для определения концентрации вирусной РНК методом ОТ-ПЦР-РВ в 4 повторах).
Статистическая обработка данных
Статистическую обработку данных проводили с использованием программного обеспечения Graphpad Prism v.5.03 и пакета RStudio (version 1.3.1093). Для оценки выживаемости использовали нелинейную четырехпараметрическую логистическую регрессию (пакет drc). Достоверность разницы выживаемости обработанных препаратами клеток с клеточным контролем определяли с использованием U-критерия Манна–Уитни при 99% доверительном интервале.
При использовании статистических процедур различия считали статистически значимыми при p ≤ 0,05.
Результаты
Оценка цитотоксичности БМПА с определением МПК и ЦТД50
В первой серии опытов оценивали цитотоксичность препарата с определением МПК и ЦТД50 в культуре клеток Vero. Исследуемые концентрации препарата (0,64; 0,32; 0,16; 0,08; 0,04; 0,02; 0,01; 0,005 и 0,0025%) вносили в клетки и инкубировали в течение 5 сут. Результаты визуального учета, а также колориметрического МТТ-теста показали, что все изученные концентрации препарата являлись токсичными для клеток и вызывали гибель более 90% из них (табл. 1).

Учитывая короткое время контакта мирамистина со слизистой дыхательных путей, в следующей серии экспериментов мы модифицировали методику определения выживаемости клеток, сократив контакт препарата с ними. Разведения препарата вносили в клетки, инкубировали 60 мин., после чего препарат удаляли, монослой клеток дважды отмывали, вносили поддерживающую среду и инкубировали в течение 3 сут. Данные микроскопического исследования монослоя на 3-и сутки после внесения препарата были подтверждены результатами МТТ-теста. Значения МПК и ЦТД50 для БМПА в культуре клеток Vero, выведенные из кривых «доза–ответ», составили 0,005% и 0,0091 ± 0,002% соответственно (рис. 1).

Оценка вирулицидной активности БМПА
Вирулицидное действие БМПА в отношении вируса SARS-CoV-2 изучали в культуре клеток Vero путем титрования смеси разведений препарата и вируса в 2 независимых опытах (табл. 2).
Полученные данные показывают, что БМПА в концентрациях 0.00015– 0,0005% не оказывал действия на инфекционную активность вируса, в концентрациях 0,00125–0,0025% не инактивировал вирус или обеспечивал неполную инактивацию. Увеличение концентрации БМПА до 0,005–0,01% воспроизводимо приводило к полному инактивирующему воздействию на вирус, снижая его титр в препарате с 5,0 lg ТЦИД50/мл до недетектируемых значений. Эти данные были уточнены и дополнены при изучении вирулицидной активности БМПА в наиболее эффективных из изученных концентраций (0,01, 0,005 и 0.0025%), для чего их смешивали с вирусом, вносили в культуру клеток Vero и инкубировали в течение 2 сут. Оценка вирулицидной активности препарата методом количественной ОТ-ПЦР-РВ со специфическими праймерами и по инфекционному титру вируса показала, что в вирусном контроле наблюдался достоверный прирост вирусной РНК и титра вируса между 1-ми и 2-ми сутками (рис. 2), в то время как вирус, инкубированный с БМПА, ни в одной из концентраций такого прироста не показал.
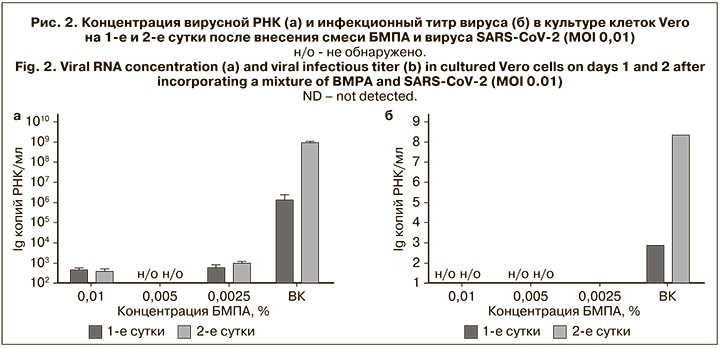
Более того, титр вируса во всех образцах, инкубированных с БМПА, был ниже предела чувствительности, а вирусная РНК в этих образцах определилась на пределе чувствительности метода ОТ-ПЦР-РВ. Таким образом, полученные результаты подтверждают полную инактивацию вируса в диапазоне концентраций БМПА 0,01–0,0025%. Важно отметить, что концентрации 0,005 и 0,00125% являются полностью нетоксичными для клеток Vero.
Обсуждение
Применение антисептических препаратов местного действия рекомендовано для лечения и профилактики новой коронавирусной инфекции, что отмечено во временных методических рекомендациях «Профилактика, диагностика и лечение коронавирусной инфекции COVID-19» [21]. В настоящей работе мы изучали эффективность одного из них в отношении инфекционной активности коронавируса SARS-CoV-2 in vitro. Установлено, что мирамистин обладает вирулицидной активностью в отношении коронавируса SARS-CoV-2, вызывая его полную инактивацию. Выявленная активность проявляется в концентрациях, соответствующих концентрации БМПА в этом препарате (0,01%), и менее (0,005 и 0,0025%). Несмотря на то что эти данные получены in vitro, они важны, поскольку отличительной особенностью препаратов для местного применения, к которым относится мирамистин, является непосредственный контакт действующего вещества с тканью, где происходит размножение вируса. Препарат обладает низкой токсичностью, и выявленные нами эффективные концентрации не являются токсичными в культуре клеток Vero, использованных для исследования. Однако первичное изучение его цитотоксичности по стандартной методике показало, что в диапазоне концентраций от 0,0025 до 0,64% при инкубации с препаратом в течение 5 сут. он обладает цитотоксичностью, вызывая гибель клеток. Поскольку в клинической практике мирамистин контактирует со слизистой оболочкой дыхательных путей в течение короткого времени, мы использовали модифицированную методику с преинкубацией клеток с препаратом в течение 60 мин. Кроме того, при интраназальном применении действующее вещество препарата попадает в среду с высокой концентрацией белка и других высокомолекулярных соединений, тогда как в культуральном тесте используется среда без сыворотки, что также может служить причиной выявленной в первых экспериментах повышенной цитотоксичности препарата.
Полученные данные о вирулицидной активности мирамистина в отношении SARS-CoV-2 важны для применения его в лечении и профилактике COVID-19 и его осложнений в нескольких аспектах. Активность препарата в отношении вируса SARS-CoV-2, вызывающего COVID-19, а также полученные ранее данные о его вирулицидной активности в отношении наиболее распространенного сезонного коронавируса ОС43 позволяют предположить отсутствие у него штаммовой специфичности в отношении различных коронавирусов [13]. Препарат обладает также вирулицидной активностью в отношении ряда респираторных вирусов, включая вирус гриппа (H3N2), аденовирусы, ECHO 6-го типа, Коксаки В1 и В6 [13, 17]. Широта спектра действия мирамистина в отношении ряда возбудителей респираторных вирусных инфекций позволяет рекомендовать его к применению без проведения диагностики. Еще одним важным аспектом является антимикробное действие препарата в отношении грамположительных и грамотрицательных бактерий [13–17], поскольку известно, что инфекция SARS-CoV-2 часто приводит к бактериальным осложнениям, среди которых наиболее распространены ЛОР-патологии [12, 22]. Совокупность этих факторов, наряду с полученными нами данными о вирулицидной активности мирамистина в отношении коронавируса SARS-CoV-2, доказывает обоснованность его применения для борьбы с COVID-19.
Заключение
Проведенное исследование показало, что оригинальная субстанция препарата мирамистин® (ООО «ИНФАМЕД») обладает выраженной вирулицидной активностью в отношении коронавируса SARS-CoV-2, полностью подавляя его инфекционность в концентрации 0,005% и выше. Путем титрования вируса и в вирусспецифической реакции ОТ-ПЦР-РВ подтверждена полная его инактивация в диапазоне концентраций 0.01–0.0025%. Таким образом, субстанция БМПА в условиях in vitro проявляет выраженную вирулицидную активность в концентрациях, соответствующих концентрации БМПА в препарате мирамистин (0,01%), и менее (0,005 и 0,0025%).


