Острые респираторные вирусные инфекции (ОРВИ) являются наиболее распространенной группой заболеваний и занимают первое место в структуре инфекционных болезней [1]. По данным Роспотребнадзора, в Российской Федерации на долю ОРВИ ежегодно приходится до 90% от всей инфекционной патологии, что составляет 27–40 млн случаев [2]. Общий экономический ущерб от ОРВИ в РФ, по разным источникам, может составлять до 100 млрд руб. ежегодно, что составляет 86% ущерба от всей инфекционной патологии [3, 4]. По данным литературы известно, что респираторные вирусы провоцируют до 80% случаев обострения бронхиальной астмы и до 60% обострений хронической обструктивной болезни легких [5]. Помимо этого от осложнений вследствие перенесенных ОРВИ в мире ежегодно регистрируется около 3,9 млн летальных исходов [6].
В эпидемический сезон 2015/2016 гг. преобладали вирусы гриппа А (H1N1), на спаде заболеваемости увеличилась циркуляция вирусов гриппа В и других ОРВИ. Заболеваемость ОРВИ была в несколько раз выше по сравнению с предыдущим сезоном, ее показатель приблизился к показателю 2009/2010 гг. (417,4 на 100 тыс. населения). Однако эпидемический сезон 2015/2016 гг. характеризуется более благоприятным течением ОРВИ и снижением летальности по сравнению с 2009/2010 гг. [7]. Такая клинико-эпидемиологическая картина обусловлена повышением роли вакцинопрофилактики гриппа и ростом иммунной прослойки населения. Так, по данным доклада руководителя Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека А.Ю. Поповой на VIII Ежегодном Всероссийском конгрессе по инфекционным болезням, в эпидемический сезон 2015/2016 гг. в РФ было привито 45 млн человек (31,3% населения), в том числе около 26 млн детей. Таким образом, в связи с высокой контагиозностью вирусов, отсутствием специфической профилактики и этиотропного лечения ОРВИ (кроме гриппа) данная группа заболеваний остается актуальной медико-социальной и экономической проблемой. Но, несмотря на разнообразие препаратов, применяемых для профилактики и лечения, ОРВИ остаются мало контролируемыми инфекциями [8].
На сегодняшний день для неспецифической профилактики и лечения ОРВИ используются лекарственные средства с разным механизмом действия. Согласно «Рекомендациям по диагностике и лечению ОРВИ у взрослых больных» (2014) [9], для терапии ОРВИ применяются противовирусные препараты умифеновир (арбидол) (регистрационный номер ЛСР-003900/07; ОАО «Фармстандарт-Томскхимфарм», Россия) и кагоцел (регистрационный номер ЛСР N002027/01; ООО «НИАРМЕДИК ПЛЮС», Россия) в стандартных дозах [10]. Лекарственные средства относятся к клинико-фармакологической группе «Прочие противовирусные препараты».
Представляется интересным сравнительный анализ эффективности разных противовирусных препаратов, наиболее часто используемых в практике для лечения больных ОРВИ.
Целью исследования явилась сравнительная оценка клинической эффективности противовирусных препаратов умифеновир и кагоцел в комплексной терапии осложненных форм ОРВИ у невакцинированных больных.
Материалы и методы
В эпидемический сезон 2015/2016 гг. в условиях инфекционного стационара под наблюдением находились 30 пациентов с осложненными формами ОРВИ, которым не проводили сезонной вакцинопрофилактики. В группе наблюдения были больные в возрасте от 18 до 60 лет, из них 16 (53%) мужчин и 14 (47%) женщин. 6 (20%) больных были в возрасте от 18 до 30 лет, 15 (50%) – от 31 до 45 лет, 9 (30%) – от 46 до 60 лет. На догоспитальном этапе 57% поступивших пациентов получали симптоматическую терапию, из них 11% принимали антибактериальную терапию. По критериям исключения в группы наблюдения не взяты пациенты, получавшие противовирусные препараты в течение месяца до госпитализации.
Пациентам проведено комплексное обследование, включающее клинический и биохимический анализы крови, электролиты крови (калий, натрий, хлор, кальций), общий анализ мочи, иммунохроматографический тест (ИХЭТ), с использованием тест-систем Influenza A+B («Vegal Farmacentica S.L.», Испания), посев на флору со слизистой оболочки носа/зева с определением чувствительности к антибиотикам, пульсоксиметрию, рентгенографию органов грудной клетки, электрокардиографию.
Согласно стандартам лечения, в условиях стационара в эпидемический сезон использовали умифеновир и кагоцел [9–11]. Препараты относятся к разным группам противовирусных лекарственных средств, но имеют сходный механизм лечебного воздействия. Умифеновир оказывает противовирусное действие и стимулирует выработку интерферонов в организме человека. На его эффективность влияет функциональное состояние печени пациента: после метаболизма в печени компоненты умифеновира приобретают новые свойства и оказывают более выраженный терапевтический эффект. Активность кагоцела не зависит от метаболизма в печени, что позволяет применять его при лечении пациентов с сопутствующими гепатитами, циррозами печени. При лечении тяжелых вирусных инфекций кагоцел и умифеновир рекомендуется применять совместно, так как компоненты препаратов усиливают действие друг друга, потенцируя противовирусный эффект. При применении кагоцела несколько чаще отмечаются аллергические реакции у детей. Стоимость препаратов в аптечной сети находится в одном ценовом диапазоне.
Статистический анализ полученных данных проводили с использованием пакетов прикладных программ Statistica 6.0. Результаты сравнений считались статистически значимыми при р ≤ 0,05.
Результаты и обсуждение
Для сравнительной оценки эффективности противовирусных препаратов была проведена рандомизация методом случайной выборки (четные и нечетные дни недели). Пациенты 1-й группы (n = 15) получали умифеновир по 200 мг 4 раза в сутки в течение 5 дней. Пациентам 2-й группы (n = 15) назначали кагоцел по 24 мг 3 раза в сутки в первые 2 дня, а в последующие 2 дня – по 12 мг 3 раза в сутки, согласно инструкции. Сформированные группы пациентов не имели гендерных и возрастных различий и были сопоставимы по клиническим и лабораторным данным. Всем пациентам проводили антибактериальную терапию препаратами цефалоспоринового ряда и симптоматическую терапию (муколитики и антигистаминные препараты).
В процессе наблюдения и лечения проводили ежедневные осмотры пациентов, регистрировали субъективные жалобы, выясняли переносимость лекарственных препаратов и возможные нежелательные явления терапии, 2 раза в сутки проводили термометрию и пульсоксиметрию.
По результатам ИХЭТ у пациентов тест на грипп был отрицательный, в посевах мокроты у троих из них обнаружен Streptococcus pneumoniae, у двоих – Staphylococcus aureus. Все пациенты госпитализированы в среднем на 3–4-е сутки от момента заболевания с жалобами на лихорадку, озноб, слабость, ломоту в теле, головную боль, кашель, ринорею, заложенность носа, першение и боль в горле, чихание. У 22 (73%) пациентов выявлен бронхит, у 8 (27%) – пневмония. В общем анализе крови количество лейкоцитов у больных с ОРВИ, осложненной пневмониями, – до 9,1 ± 1,1 х 109, у больных ОРВИ с бронхитом – 8,4 ± 0,7 х 109.
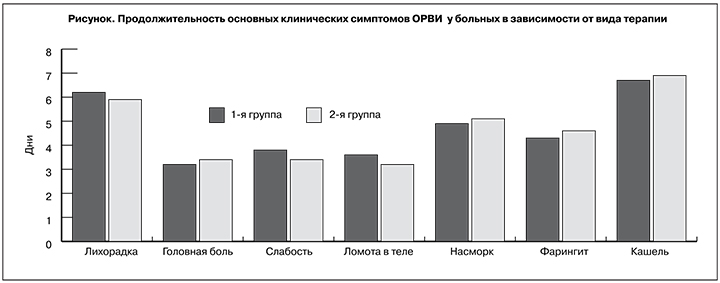
Эффективность терапии оценивали по длительности сохранения симптомов ОРВИ (см. рисунок).
В 1-й группе средняя продолжительность заболевания составила 6,1 ± 0,6 койко-дня, во 2-й – 6,3 ± 0,4. Достоверных различий в показателях общего анализа крови и пульсооксиметрии у больных двух групп на фоне терапии нет. В ходе исследования не было зарегистрировано случаев нежелательных побочных явлений применения препаратов, повлекших за собой ухудшение состояния и самочувствия, что потребовало бы отмены или замены препаратов.
Статистически значимых различий в эффективности влияния исследуемых препаратов на интоксикационный синдром и катаральные явления у пациентов сравниваемых групп не отмечено. По окончании курса лечения у всех пациентов наблюдалась положительная динамика. Отчетливый клинический эффект отмечен в отношении катарально-респираторного синдрома, сокращения лихорадочного периода, разрешения пневмонии (по данным рентгенологического исследования) в обеих группах наблюдения. Более быстрое клиническое восстановление пациентов с пневмониями наблюдалось во 2-й группе (2 случая), но эти данные статистически не достоверны. При анализе лабораторных данных в динамике достоверных различий показателей у больных обеих групп не выявлено.
Таким образом, в проведенном сравнительном анализе клинической эффективности и безопасности терапии осложненных форм ОРВИ у непривитых больных препаратами умифеновир и кагоцел получены сопоставимые результаты.



