Распространенность хронического гепатита С (ХГС) в мире постоянно растет, и, согласно оценкам Всемирной организации здравоохранения (ВОЗ), на данный момент число заболевших превышает 185 млн. Около 350 000 человек ежегодно умирают от развившихся на фоне ХГС цирроза печени (ЦП) и гепатоцеллюлярной карциномы. Эпидемия гепатита С – одна из самых серьезных угроз для общественного здравоохранения, с последствиями которой многим странам предстоит иметь дело еще в течение нескольких десятилетий [1].
Вирус гепатита С (ВГС) – один из самых сложных вирусов с гетерогенным геномом. Специалисты насчитывают 11 его генотипов и подтипов, которые в разной степени распространены по странам и регионам мира. Наиболее распространены генотипы 1а и 1b: в мире ими инфицировано около 60% больных ХГС, подавляющее большинство – в странах Европы и Северной Америки. Генотип 3 является эндемичным для Юго-Восточной Азии [2]. В Российской Федерации распространены (в порядке убывания) генотипы 1, 3, 2. Среди подтипов чаще встречается 1b, чем 1а (как и в европейской популяции), а также 3а. Генотипы 4–6 практически не встречаются в популяции Российской Федерации.
Противовирусная терапия (ПВТ) ХГС существенно изменилась за последние 17 лет. В 1998 г. Управление по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) впервые одобрило комбинацию терапии интерфероном α-2b (ИФН-α-2b), вводимым подкожно 3 раза в неделю, с рибавирином (РБВ). Это стало стандартной схемой лечения, дающей устойчивый вирусный ответ (УВО) в 38–43% случаев, с существенной разницей в результатах, обусловленной генотипом ВГС [3].
В 2001–2002 гг. появились 2 новые формы интерферона в пегилированном виде (ПегИФН): ПегИФН-α-2а и ПегИФН-α-2b, которые позволили улучшить показатели до 42–51% при генотипах 1 и 4 и до 68–78% – при генотипах 2 или 3 и сократить число инъекций до одного раза в неделю [4–6].
Терапия ХГС ПегИФН-α-2а или ПегИФН-α-2b и РБВ в течение 24–72 недель на долгое время была признана «золотым стандартом» лечения. Однако низкие показатели эффективности у ранее не леченых и особенно у потерпевших неудачу ПВТ пациентов диктовали необходимость поиска более эффективных методов лечения.
Самым драматичным образом ситуация складывалась для пациентов с выраженным фиброзом печени (F3 по METAVIR) и компенсированным ЦП (класс А по классификации Чайлда–Пью), у которых ещё можно предотвратить прогрессирование заболевания до более тяжёлых стадий, но эффективность традиционного лечения не превышала 23,6% по критерию достижения УВО [7].
В 2011 г. FDA и Европейской службой по надзору в сфере лекарственных средств были одобрены и стали доступными для лечения ХГС, вызванного ВГС генотипа 1, два пероральных ингибитора протеазы ВГС NS3/4A – телапревир и боцепревир, применяемые в комбинации с ПегИФН и РБВ. В России эти схемы лечения были одобрены и стали доступны в течение последующих двух лет. Проведенные исследования продемонстрировали высокую эффективность ПВТ, включавшей, помимо ПегИФН и РБВ, ингибитор протеазы. Так, у больных ХГС, вызванным ВГС генотипа 1, ранее не получавших терапии, частота УВО составила 67–70% [8, 9].
 Однако тройная терапия, включающая боцепревир или телапревир, имела ряд существенных недостатков [10–14]. Сами препараты могли вызывать серьезные побочные эффекты, среди которых наиболее частой являлась анемия [15]. В клинических исследованиях нежелательные реакции (утомляемость, сыпь, зуд, анемия и тошнота) чаще наблюдались в группе тройной терапии по сравнению с группой, получавшей комбинацию ПегИФН и РБВ. Необходимость отмены лечения из-за побочных эффектов в целом и серьезных нежелательных явлений также чаще возникала в группе тройной терапии [10, 11].
Однако тройная терапия, включающая боцепревир или телапревир, имела ряд существенных недостатков [10–14]. Сами препараты могли вызывать серьезные побочные эффекты, среди которых наиболее частой являлась анемия [15]. В клинических исследованиях нежелательные реакции (утомляемость, сыпь, зуд, анемия и тошнота) чаще наблюдались в группе тройной терапии по сравнению с группой, получавшей комбинацию ПегИФН и РБВ. Необходимость отмены лечения из-за побочных эффектов в целом и серьезных нежелательных явлений также чаще возникала в группе тройной терапии [10, 11].
В конце ноября 2013 г. в США был одобрен к медицинскому применению ингибитор протеазы NS3/4A второго поколения симепревир, имеющий более благоприятный профиль безопасности по сравнению с ингибиторами протеазы первого поколения. В клинических исследованиях УВО при применении симепревира в составе тройной терапии наблюдался у 93–96% больных, ранее не получавших лечения [16]. Среди больных, не ответивших на предыдущую ПВТ, УВО наблюдался в 68–79% случаев [17].
В 2014–2015 гг. произошел прорыв в лечении ХГС, ознаменовавшийся выходом на рынок сразу нескольких препаратов прямого противовирусного действия (ПППД): софосбувира, даклатасвира, ледипасвира, асунапревира и комбинаций омбитасвира, паритапревира, ритонавира и дасабувира. Появление новых препаратов сделало возможным проведение безинтерфероновой терапии более короткими курсами и повысить эффективность ПВТ ХГС более 95% [18–22].
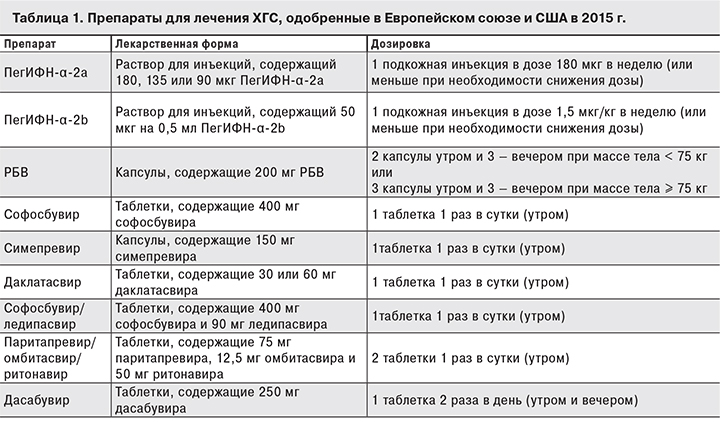
Таким образом, к 2016 г. в ПВТ ХГС существует 2 стратегических терапевтических направления: первое основано на применении препаратов ИФН, второе включает использование только препаратов прямого противовирусного действия. Препараты для лечения ХГС, одобренные в Европейском союзе и США в 2015 г., представлены в табл 1.
Международный опыт лечения ХГС к настоящему времени суммирован в международных рекомендациях двух крупнейших медицинских сообществ, занимающихся проблемами изучения болезней печени: Европейской (European Association for the Study of the Liver – EASL) и Американской (American Association for the Study of Liver Diseases – AASLD) ассоциаций. В 2014 г. ВОЗ впервые выпустила рекомендации по лечению гепатита С. В России клинические рекомендации по лечению гепатита С, обновленные в 2014 г., представлены Российской гастроэнтерологической ассоциацией совместно с Российским обществом по изучению печени (РОПИП).
В нашей статье мы бы хотели провести сравнительную характеристику основных международных и российских рекомендаций по лечению пациентов с ХГС.
ПВТ пациентов с ХГС, вызванным ВГС генотипа 1
Согласно европейским рекомендациям, для пациентов с ХГС, инфицированных ВГС генотипа 1, предусмотрено 6 вариантов лечения, включая 2 схемы с ИФН и 4 схемы без них.
Интерферонсодержащие схемы включают комбинацию ПегИФН-α и РБВ в сочетании с софосбувиром или симепревиром. Курс лечения с применением софосбувира – фиксированный и составляет 12 недель. При включении в схему ПВТ ингибитора протеазы симепревира следует назначать его в течение 12 недель, затем отдельно следует вводить ПегИФН-α и РБВ в течение еще 12 или 36 недель (общая продолжительность лечения – 24 или 48 недель в зависимости от ответа на предыдущее лечение и/или наличие/отсутствие ЦП).
К безинтерфероновым схемам ПВТ при ХГС, вызванном ВГС генотипа 1, согласно рекомендациям Европейского сообщества, относятся: комбинация софосбувир/ледипасвир в одной таблетке, комбинация софосбувир/симепревир, комбинация софосбувир/даклатасвир и комбинация омбитасвир/паритапревир/ритонавир в одной таблетке и дасабувир («3D-терапия»). Данные комбинации препаратов применяются в течение 12 или 24 недель с РБВ или без него (в зависимости от наличия/отсутствия ЦП, а для режима «3D» еще и в зависимости от подтипа генотипа ВГС – 1а или1b) [23].
В американских рекомендациях выбор препаратов для терапии ХГС, вызванного ВГС генотипа 1, несколько уже. Американские эксперты не рекомендуют применение интерферонсодержащих схем для данного генотипа вируса. Безинтерфероновые схемы лечения полностью совпадают с рекомендациями Европейского сообщества. В 2016 г. рекомендации AASLD пополнились еще одной схемой терапии ХГС, вызванного ВГС генотипа 1, – фиксированной комбинацией элбасвир/гразопревир с добавлением РБВ или без него в течение 12 или 16 недель (в зависимости от наличия/отсутствия ЦП) [24].
Согласно рекомендациям ВОЗ, для пациентов, инфицированных ВГС генотипа 1, предусмотрены следующие схемы лечения: ПегИФН и РБВ в течение 24–48 недель, Пег-ИФН и РБВ в комбинации с телапревиром, боцепревиром или симепревиром в течение 24–48 недель или в комбинации с софосбувиром в течение 12 недель и комбинация софосбувир/РБВ в течение 24 недель (при непереносимости ИФН) [1].
В Российской Федерации, согласно рекомендациям 2014 г., для пациентов с ВГС генотипа 1 предпочтительной схемой ПВТ является тройная терапия, включающая ПегИФН или ЦеПегИФН-α-2b, РБВ и ингибитор протеазы ВГС (телапревир, боцепревир или симепревир) в течение 24–48 недель [25].
ПВТ пациентов с ХГС, вызванным ВГС генотипа 3
При выборе препаратов для ПВТ ХГС у пациентов, инфицированных ВГС генотипа 3, мнения экспертов EASL и AASLD совпали.
Согласно европейским и американским рекомендациям, для таких пациентов доступны 3 варианта лечения: комбинация ПегИНФ-α/РБВ/софосбувир в течение 12 недель, комбинация РБВ/софосбувир в течение 24 недель и комбинация софосбувир/даклатасвир в течение 12 недель (пациенты с ЦП должны получать данную комбинацию с РБВ в течение 24 недель) [23, 24].
Согласно рекомендациям ВОЗ, для пациентов, инфицированных ВГС генотипа 3, предусмотрены следующие схемы лечения: комбинация ПегИФН/РБВ в течение 24–48 недель, комбинация софосбувир/РБВ в течение 24 недель или комбинация софосбувир/РБВ/ПегИФН в течение 12 недель [1].
Согласно российским рекомендациям, в качестве терапии первой линии у пациентов с ХГС, вызванным ВГС генотипов 2 и 3, рассматриваются ПегИФН-α или ЦеПегИФН-α-2b в сочетании с РБВ в течение 24 недель. [25] В России применяется также комбинированная терапия ХГС стандартным ИФН-α в сочетании с РБВ. Длительность лечения аналогична таковой при применении ПегИФН. Однако, говорят российские эксперты, необходимо учитывать, что эффективность такой схемы лечения ниже, чем при применении ПегИФН в сочетании с РБВ. Тем не менее в условиях ограниченного экономического ресурса, на основании полученного в России опыта [26–29] существует мнение, что этот вид ПВТ может применяться, следуя принципу «терапия согласно вирусологическому ответу» для особой группы пациентов (возраст моложе 40 лет, отсутствие выраженного фиброза/ЦП, отсутствие сопутствующих заболеваний и факторов неблагоприятного прогноза в достижении УВО) [25].
ПВТ ХГС у пациентов с коинфекцией ВИЧ/ВГС
По сравнению с моноинфекцией ВГС, пациенты с сочетанной инфекцией ВГС/ВИЧ имеют более высокий уровень РНК ВГС в крови, более быстрое прогрессирование заболевания до ЦП и гепатоцеллюлярной карциномы [30–32].
Лица с коинфекцией ВИЧ/ВГС хуже отвечают на терапию ПэгИФН и РБВ, что во многом объясняется более высоким исходным уровнем РНК ВГС в их крови [33, 34].
Однако с появлением ПППД различий в ответах на ПВТ ХГС при моно- и коинфекции не было [35, 36].
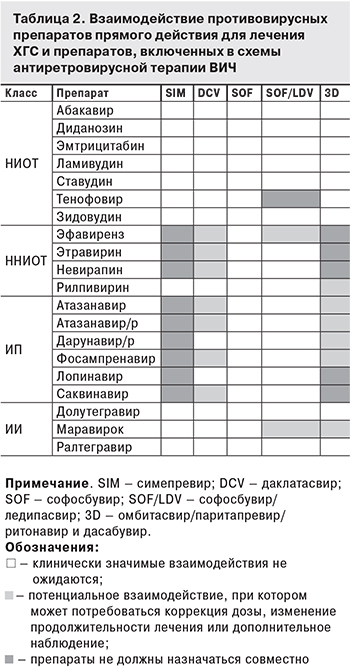
Таким образом, согласно общему мнению экспертов EASL, AASLD и ВОЗ, рекомендации по лечению ХГС у пациентов с коинфекцией ВИЧ/ВГС ровно такие же, как и для пациентов с моноинфекцией ВГС. Необходимо только учитывать межлекарственные взаимодействия с антиретровирусными препаратами [1, 23, 24] (табл. 2).
Обозначения:
- клинически значимые взаимодействия не ожидаются;
- потенциальное взаимодействие, при котором может потребоваться коррекция дозы, изменение продолжительности лечения или дополнительное наблюдение;
- препараты не должны назначаться совместно
Согласно российским рекомендациям, стандартом терапии ХГС у ВИЧ-инфицированных пациентов (ВГС генотипов 2 и 3) является использование ПегИФН и РБВ. Курс лечения – 24–72 недель [25, 37].
Препаратом выбора для тройной схемы терапии при ХГС, вызванном ВГС генопипа 1, является симепревир вследствие преимущественных режима дозирования и профиля безопасности. Коррекции дозы симепревира у таких пациентов не требуется, необходимо только учитывать межлекарственные взаимодействия [25]. А согласно российским Национальным рекомендациям по диспансерному наблюдению и лечению больных ВИЧ-инфекцией, обновленным в 2015 г. [37], больным с коинфекцией ВИЧ/ВГС для терапии ХГС, вызванного ВГС генотипа 1, в качестве схемы выбора рекомендуется режим «3D» в сочетании с РБВ. Длительность терапии – 12 недель (для генотипа 1а с ЦП – 24 недели).
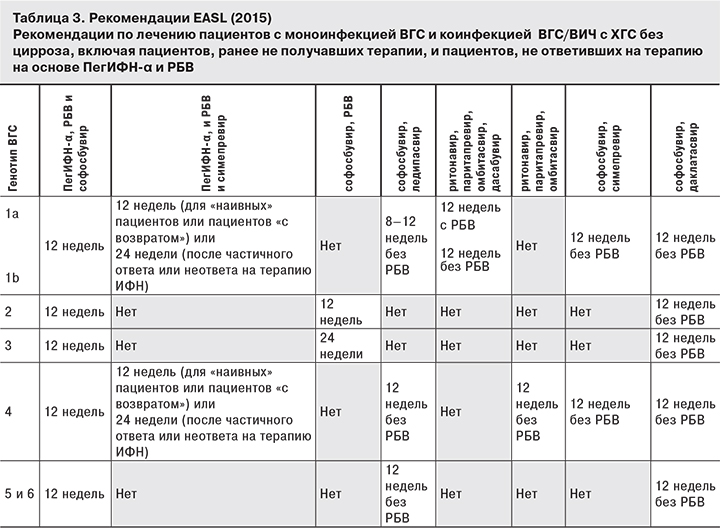
При сравнении основных международных рекомендаций по лечению ХГС становится очевидным, что большинство стран переходит на безинтерфероновые схемы терапии. В американских рекомендациях интерфероновую схему используют только при ВГС генотипа 3, и то как альтернативный вариант лечения. Не исключено, что ПегИФН в США в скором времени исключат из реестра противовирусных препаратов для лечения ХГС. Эксперты Европейской ассоциации несколько более консервативны: из 8 схем лечения ХГС 2 еще включают ИФН (табл. 3).
В рекомендациях ВОЗ большинство схем ПВТ ХГС базируются на применении ПегИФН, и лишь одна включает только препараты прямого противовирусного действия.
Если говорить о российских рекомендациях, то в редакции 2014 г. они вообще не содержат безинтерфероновых схем, поскольку такие схемы были зарегистрированы в Российской Федерации совсем недавно, и на момент написания рекомендаций их в России еще не было.
В 2015 г. в России зарегистрированы такие препараты прямого противовирусного действия, как даклатасвир, асунапревир, комбинация омбитасвир/паритапревир/ритонавир и дасабувир. В марте 2016 г. зарегистрирован софосбувир.
В Перечень жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП) в Российской Федерации для терапии ХГС входят такие препараты, как ПегИФН-α-2а, ПегИФН-α-2b, ЦеПегИФН-α-2b и РБВ. Препаратов прямого противовирусного действия в списке ЖНВЛП на 2016 г. нет.
Таким образом, при анализе рекомендаций по лечению ХГС, принятых в разных странах мира, становится очевидным, что ПППД становятся основным средством лечения ХГС.



