В России увеличивается число пациентов с ВИЧ-инфекцией. Если раньше большую часть из них составляли мужчины, то в настоящее время растет число случаев заболевания и среди женщин, особенно фертильного возраста, а профилактика вертикальной передачи остается одной из наиболее важных медико-социальных проблем, связанных с ВИЧ-инфекцией [1–4]. Так, с 2000 по 2012 г. в Саратовской области относительные показатели заболеваемости ВИЧ-инфекцией среди женщин увеличились более чем в 2,5 раза, при этом значительно выросло число беременных с ВИЧ и родов среди ВИЧ-инфицированных. В 1996–2012 гг. на территории Саратовской области зарегистрировано 1797 детей, рожденных ВИЧ-инфицированными матерями. За этот период мероприятия по профилактике существенно изменились: значительно корректировались ее сроки и объем. Необходимо отметить, что за последние годы возможности антиретровирусной терапии (АВТ) существенно расширились за счет как новых классов, так и отдельных препаратов. Вместе с тем лечение беременных и химиопрофилактика (ХП) вертикальной передачи остаются одной из наиболее сложных проблем, что связано, в первую очередь, с этически обусловленными ограничениями проведения исследований по изучению эффективности и безопасности новых препаратов у беременных. При формировании клинических рекомендаций по использованию медикаментов для АРТ и ХП вертикальной передачи ВИЧ помимо обычных требований к препаратам учитываются также данные о возможном негативном влиянии лекарственных средств на плод, в том числе о частоте врожденных пороков развития на фоне приема того или иного средства. В этих условиях сообщения о клинических случаях использования тех или иных препаратов являются очень ценными и актуальными.
С 2013 г. в перечень предпочтительных препаратов при ведении ВИЧ-инфицированных беременных из ингибиторов протеазы (ИП), наряду с лопинавиром (LPV/r), включен атазанавир (ATV), который сочетается с а зидовудином (ZDV) и ламивудином (3TC). Такие изменения стали возможны после ряда исследований безопасности применения препарата у беременных. Как альтернативные средства в отдельных случаях рассматриваются абакавир в комбинации с ламивудином (ABC/3TC), фосфазид (Ф-АЗТ), невирапин (NVP), дарунавир или саквинавир, усиленные ритонавиром (DRV/r, SQV/r). В особых ситуациях возможно применение тенофовира (TDF) и ралтегравира (RAL).
Решение о выборе схемы терапии у ВИЧ-позитивных беременных должно основываться на клинической ситуации, имеющемся опыте, доступности препаратов, а также потенциальной токсичности комбинаций различных средств.
На базе Саратовского областного центра профилактики и борьбы со СПИД (далее – Центр СПИДа) было проведено исследование эффективности различных вариантов ХП вертикальной передачии ВИЧ-инфекции.
Материалы и методы
Методом сплошной выборки проведен ретроспективный анализ 1355 случаев рождения детей ВИЧ-инфицированными женщинами, состоявшими на диспансерном учете в Центре СПИДа за период с 1996 по 2010 г. В исследование были включены дети в возрасте 18 месяцев и старше.
С учетом варианта ведения беременности были выделены несколько групп:
- дети с трехэтапной ХП (п = 903 или 66,7%);
- дети с экстренной ХП вертикальной передачи ВИЧ (п = 284 или 21,2%);
- дети, рожденные ВИЧ-позитивными матерями, которым АРТ была назначена до наступления беременности (п = 19 или 1,4%).
- дети, матерям которых ХП ВИЧ-инфекции не проводилась (п = 130 или 9,6%).
Антиретровирусную химопрофилактику (АРХП) вертикальной передачи ВИЧ от матери ребенку проводили согласно действующим на период ведения беременной нормативным документам и методическим рекомендациям, принятым в Российской Федерации. В 65,9% случаев применяли схему: 2 НИОТ (ZDV, 3TC) в комбинации с бустированными ИП (LPV/r, ATV/r). Реже (в 12,4% случаев) использовали схему: 2 НИОТ + 1 ННИОТ (NVP), а также схемы с одним или двумя препаратами (21,7% случаев). Отсутствие АРХП в группе из 130 человек было обусловлено ограниченным доступом к антиретровирусным препаратам (АРВП) в начале эпидемии ВИЧ-инфекции, а также отсутствием требования законодательства о тестировании беременных на ВИЧ. Экстренная ХП были связаны с несвоевременным обращением и выявлением беременных с ВИЧ-инфекцией. В ряде случаев причинами отклонений в проведении АРХП были домашние роды (1 случай), сокрытие диагноза в родильном доме (6 случаев), отказ женщины от ХП (3 случая).
Для математического анализа полученных результатов использовали параметрические и непараметрические методы. Для сравнения двух независимых групп по одному признаку использовали критерий Колмогорова–Смирнова. При сравнении трех независимых групп по одному признаку достоверность различий оценивали по критерию Пирсона (χ2) с поправкой Йетса. Сравнение двух зависимых групп по одному признаку осуществляли с использованием критерия Вилкоксона. При обработке результатов исследования использовали пакеты прикладных программ Statistica 10.0 и Microsoft Exel for Windows 7.0.
Результаты и обсуждение
Возраст ВИЧ-инфицированных беременных колебался от 18 до 44 лет, средний возраст на момент родов составил 23,5 ± 2,8 года.
Большинство (58,7%) состоявших на учете женщин были инфицированы в результате полового контакта. Вторым по частоте являлся парентеральный путь передачи – 26,1% случаев, возможное сочетание полового и парентерального пути встречалось в 13,3% случаев, неустановленный путь передачи зафиксирован в 1,9% случаев. Внутривенное употребление психоактивных веществ отмечено в анамнезе у 39,5% женщин, табакокурение – у 33,3%, алкоголизм – у 2,3%, отсутствие вредных привычек – у 24,9%.
50,9% женщин находились на стадии 3 ВИЧ-инфекции (в соответствии с классификацией В.И. Покровского) [5]. Стадия 4А была диагностирована в 43,8% случаев (п = 585), 4Б – в 3,6% (п = 48) и 4В – в 1,7% (п = 22). Содержание CD4-лимфоцитов более 500 клеток/мкл непосредственно перед родами (за 1–3 недели) было у 51,2% женщин, менее 500 клеток/мкл – у 48,8%. Вирусная нагрузка за 1–3 недели до родов в 65,2% случаев составляла менее 400 копий/мл. Анализ вероятности вертикальной передачи в зависимости от уровня виремии и состояния иммунного ответа (CD4) не проводился.
Угроза прерывания беременности отмечена в 62,8% случаев, гестоз 2-й половины беременности – в 37,2%. У 19,7% женщин ВИЧ-инфекция сочеталась с гепатитами В и/или С, у 23,3% выявлены заболевания урогенитального тракта, у 2,3% – туберкулез.
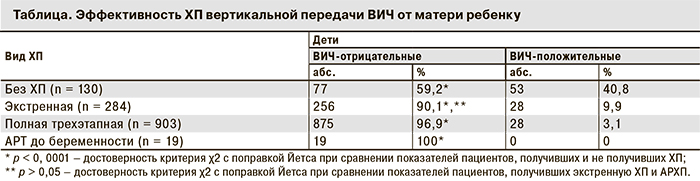
Диагноз «ВИЧ-инфекция» через 18 и более месяцев после родов был установлен 109 детям (8,2%) из 1355 проанализированных случаев родов.
При статистическом анализе закономерно очень высокими оказались показатели вертикальной передачи ВИЧ в группе детей, матерям которых ХП не проводилась – были инфицированы 53 ребенка (40,8%) из 135 (см. таблицу).
Экстренная ХП (в период родов у матери и после родов у ребенка) снизила уровень вертикальной передачи ВИЧ до 9,9% (28 детей из 284), что было достоверно ниже (p < 0,0001), чем при отсутствии приема препаратов.
Приоритетным способом ХП, применяемым в Центре СПИДа, был трехэтапный вариант с использованием нескольких препаратов, который обеспечил снижение до 3,1% риска передачи ВИЧ-инфекции по сравнению с отсутствием профилактики и экстренной ХП (p < 0,0001 в обоих случаях).
По нашим наблюдениям, все 19 случаев беременности среди пациенток с ВИЧ-инфекцией в стадии вторичных заболеваний, которые получали АРТ, включающую предпочтительные схемы [5, 6] [18 – с ИП (ATV/r, LPV/r)] завершились рождением неинфицированных детей. Таким образом, даже у женщин с ВИЧ-инфекцией в стадии вторичных заболеваний адекватные подходы к проведению ХП позволяют достичь хороших результатов в предупреждении передачи вируса ребенку.
Результаты исследования подтвердили абсолютную необходимость и целесообразность проведения трехэтапной АРХП, что позволяет радикально снизить уровень вертикальной передачи ВИЧ и успешно контролировать распространение эпидемии среди детей раннего возраста. Наши данные полностью подтверждают данные зарубежных и отечественных исследователей по проблеме передачи ВИЧ-инфекции от матери ребенку [7–9]. Важно подчеркнуть, что в соответствии с современными рекомендациями при определении высокой вирусной нагрузки у беременной ХП нужно начинать сразу после констатации уровня вирусной нагрузки [10].
Даже экстренный вариант ХП дает относительно хорошие результаты и должен обязательно применяться в соответствующих ситуациях, что также подчеркивается в многочисленных научных публикациях [11–13].
АРТ, проводимая женщине в соответствии с клиническими показаниями, позволяет при наступлении беременности обеспечить высокую вероятность рождения ВИЧ-негативного ребенка [14, 15], а по нашим данным – в 100% случаев.
Расширение списка препаратов, рекомендованных для использования у беременных, является трудоемким и длительным процессом. Как известно, ATV не так давно вошел в перечень предпочтительных препаратов для профилактики передачи ВИЧ от матери ребенку. В связи с этим публикации клинических наблюдений представляют большой интерес. Этот лекарственный препарат зарегистрирован в РФ в 2005 г. и являлся первым представителем ИП с возможностью приема 1 раз в сутки у всех категорий пациентов. Как и другие препараты из группы ИП, он обладает высокой противовирусной активностью и низким уровнем токсичности. Важным достоинством ATV является возможность одноразового приема у беременных, минимальное (для группы ИП) влияние на углеводный и липидный обмен, отсутствие необходимости изменения дозы во II и III триместре беременности.
За время применения в широкой клинической практике ATV подтвердил свою эффективность и безопасность и сегодня входит в число предпочтительных препаратов в схемах АРТ.
Поэтому мы хотели бы поделиться своим опытом применения ATV как препарата для профилактики вертикальной передачи ВИЧ.
Приводим 2 клинических случая течения беременности у ВИЧ-позитивных женщин: в первом случае женщина находилась в латентной стадии заболевания и получила АРХП, во втором – у ВИЧ-инфицированной беременность наступила на фоне АРТ.
Беременная М., 24 года. При плановом обследовании в женской консультации на сроке гестации 10 недель диагностирована ВИЧ-инфекция. Женщина была направлена в Центр СПИДа. При постановке на учет количество CD4-лимфоцитов – 496 клеток/мкл, вирусная нагрузка по результатам ПЦР – 155 772 копий/мл. Путь заражения – предположительно половой. Ориентировочные сроки инфицирования – за 4–5 лет до наступления беременности. Из сопутствующих заболеваний выявлена анемия легкой степени, латентная герпетическая инфекция.
Беременной была назначена АРХП по схеме: 3ТС 150 мг 2 раза в сутки, ZDV 300 мг 2 раза в сутки, ATV/r 300/100 мг 1 раз в сутки. В первые 2 недели приема препаратов пациентка отмечала «неприятные ощущения в области желудка», однако в дальнейшем побочных эффектов на прием АРВП не наблюдалось, приверженность к терапии высокая.
Уже через 4 недели после начала АРХП вирусная нагрузка ВИЧ снизилась до 1528 копий/мкл, уровень CD4-лимфоцитов – 507 клеток/мкл, а на 8-й неделе виремия не определялась (менее 50 копий/мл). Анемия была скорректированна препаратами железа.
Беременность на фоне приема АРХП протекала без особенностей. Периодически отмечалась небольшая тошнота.
Больная была госпитализирована в родильный дом на сроке беременности 38 недель, при этом уровень CD4-лимфоцитов составил 537 клеток/мкл, вирусная нагрузка не определялась (менее 50 копий/мл). Была выбрана консервативная тактика ведения родов. В родах на 39-й неделе беременности пациентка получила ZDV внутривенно капельно. Ребенок родился с массой тела 3050 г, оценка по шкале Апгар – 7–8 баллов. Новорожденному было назначено искусственное вскармливание и АРХП раствором ретровира в течение 6 недель. При диспансеризации в Центре СПИДа через 1,5 месяца после рождения ребенок соответствовал возрастным нормам, отклонений в физическом развитии не выявлено. В дальнейшем по развитию ребенок не отставал от сверстников.Мать строго выполняла рекомендации по искусственному вскармливанию адаптированными молочными смесями.
При диспансеризации в возрасте 18 месяцев масса тела ребенка составляла 11,3 кг; из сопутствующих заболеваний выявлена анемия легкой степени. Антитела к ВИЧ не определялись (ИФА АГ/АТ «–»). Решением врачебной комиссии ребенок снят с учета.
Больная Т., 37 лет. Состоит на учете в Центре СПИДа с 2010 г. Путь инфицирования – половой, предположительный срок заражения – 2003–2004 гг. В мае 2011 г., перед началом лечения, уровень CD4-лимфоцитов – 256 клеток/мкл, вирусная нагрузка – 408 000 копий/мл. пациентке назначена АРТ по схеме: ZDV/3ТС 300/150 мг по 1 таблетке 2 раза в сутки, эфавиренз (ЕFV) 600 мг 1 раза в сутки. Через 12 месяцев от начала терапии уровень CD4-лимфоцитов – 344 клеток/мкл, вирусная нагрузка не определяется (< 40 копий/мл). В дальнейшем приверженность к терапии снизилась, больная нерегулярно посещала Центр СПИДа,
В январе 2014 г. после выяснения факта беременности больная самостоятельно прервала прием АРВП на 2 недели. Обратилась в Центр СПИДа на сроке беременности 7–
8 недель. При обследовании уровень CD4-лимфоцитов – 320 клеток/мкл, вирусная нагрузка не определяется (< 20 копий/мл). Принято решение изменить схему АРТ с учетом вновь возникших обстоятельств и назначить ZDV/3ТС 300/150 мг по 1 таблетке 2 раза в сутки и ATV/r 300/100 мг 1 раз в сутки.
В процессе диспансерного наблюдения переносимость АРТ была удовлетворительной, приверженность – высокой, отклонения в течение беременности не наблюдались, уровень CD4-лимфоцитов колебался в пределах 332–367 клеток/мкл, виремия не выявлялась. Больная регулярно посещала акушера-гинеколога и инфекциониста.
На сроке беременности 38 недель уровень CD4-лимфоцитов составил 387 клеток/мкл, вирусная нагрузка не определялась (< 20 копий/мл). Была выбрана консервативная тактика ведения родов, осуществлена профилактика вертикальной передачи ВИЧ-инфекции ZDV.
Беременность завершилась на 39-й неделе рождением ребенка с массой тела 3250 г, оценка по шкале Апгар – 7–8 баллов. Новорожденному было назначено искусственное вскармливание и ХП раствором ретровира в течение 6 недель.
В ходе дальнейшего диспансерного наблюдения за ребенком в Центре СПИДа с 1,5 до 18 месяцев после рождения отклонений в физическом развитии не выявлено, режим искусственного вскармливания адаптированными смесями матерью соблюдался. При контроле наличия в крови антител к ВИЧ (ИФА, иммуноблот) и вируса (ПЦР двухкратно) получены отрицательные результаты. В возрасте 18 месяцев масса тела составила 10,9 кг, сопутствующих заболеваний не выявлено. На основании результатов обследования принято решение об отсутствии инфицирования ВИЧ, и ребенок снят с учета.
Таким образом, беременность является безусловным показанием для назначения ВИЧ-инфицированным женщинам ХП и продолжения АРТ, однако при подборе конкретной схемы лечения необходимо соотнести ее риск и пользу. В приведенных клинических наблюдениях использованные схемы ХП и АРТ, включающие ATV/r в комплексе с 3ТС и ZDV, обеспечили рождение свободных от ВИЧ детей без существенных отклонений в психосоматическом статусе.
Выводы
- ХП вертикальной передачи ВИЧ с применением АРВП является высокоэффективным способом предотвращения распространения инфекции среди детей раннего возраста.
- Использование оптимизированных схем АРТ у беременных с ВИЧ-инфекцией, в том числе в стадии вторичных заболеваний, в сочетании с ХП ребенку и матери в родах обеспечивает минимальную вероятность вертикальной передачи вируса ребенку.



