Escherichia coli − постоянный обитатель кишечного тракта млекопитающих и птиц. Подавляющая часть популяции E. coli являются представителями нормальной микробиоты макроорганизма, меньшая часть способна вызывать многочисленные патологические процессы у человека и животных, включая кишечные и урологические заболевания, системные поражения (бактериемию, сепсис), менингит и другие заболевания [1]. Уропатогенные Escherichia coli (УПЭК) вызывают 90% внегоспитальных и 50% госпитальных инфекций мочевыводящих путей (ИМВП) [2]. УПЭК-инфекции вызывают не только чувствительные (S), но и преимущественно резистентные (R) и множественно резистентные (MDR) штаммы [3, 4]. Фенотип MDR ассоциирован с наличием генетических детерминант, определяющих устойчивость к бета-лактамам, аминогликозидам, сульфаниламидам и другим антимикробным препаратам (АМП), а также с присутствием интегронов [5]. К генетическим детерминантам, ассоциированным с проявлением патогенных свойств УПЭК, относят гены адгезинов, токсинов, сидерофоров, протектинов и др. [5].
Штаммы УПЭК характеризуются высокой степенью генетической гетерогенности, поэтому важное эпидемиологическое значение имеет внутривидовое молекулярно-генетическое типирование, позволяющее определить принадлежность штаммов к филогенетическим группам (A, B1, B2, D, E, F или клада I), О-группам и сиквенс-типам. Совокупность указанных признаков штамма определяет клональную группу штамма E. coli [6]. Наиболее распространенной клональной группой УПЭК в мире считается O25-B2-ST131, впервые задокументированная в 2008 г. и выделенная во многих странах. Широко распространены в мире также клональные группы УПЭК D-ST405, A-CC10, O6-B2-ST73, O1/O2/O18-B2-ST95, D-ST117, O75-B2-CC14, O15-D-ST393 и O11/O17/O73/O77-D-ST69 [6–10]. Публикации об идентификации клональных групп УПЭК-штаммов, выделенных в Российской Федерации, отсутствуют.
Цель исследования – идентификация клональных групп E. coli, изолированных от пациентов с ИМВП в Российской Федерации в 2004–2019 гг., а также определение у них генов вирулентности, фено- и генотипов антибиотикорезистентности.
Материалы и методы
Использованные в данном исследовании материалы не содержат персональных данных пациентов. В соответствии с требованиями Биоэтического комитета Российской Федерации каждый пациент подписывал информированное согласие на проведение лабораторных исследований. Исследовали штаммы E. coli (n = 303), выделенные из образцов мочи пациентов с урологическими диагнозами в 2004–2019 гг. Штаммы получены из НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина (n = 161), Национального медицинского исследовательского центра акушерства, гинекологии и перинатологии им. академика В.И. Кулакова (n = 50), Московской медицинской академии им. И.М. Сеченова (ныне Первый МГМУ им. И.М. Сеченова) (n = 50), ИКБ № 1 Департамента здравоохранения Ярославской области (n = 20) и других источников (n = 22). Выделенные штаммы выращивали на плотной питательной среде «Питательная среда № 1 ГРМ-агар» (Государственный научный центр прикладной микробиологии и биотехнологии, Оболенск) в чашках Петри в течение 18–24 ч при температуре 37 °C. Культуры хранили при температуре -70 °C в водном растворе 20% глицерина. Видовую идентификацию осуществляли на основе анализа свойств при выращивании штаммов на дифференциально-диагностических средах с последующим подтверждением вида микроба на приборе MALDI-TOF Biotyper (Bruker, Karlsruhe, Германия).
Резистентность к антимикробным препаратам определяли по уровню минимальных подавляющих концентраций 9 антимикробных препаратов 5 функциональных групп: бета-лактамов (ампициллин, амоксициллин/клавуланат, цефотаксим), фторхинолонов (ципрофлоксацин, левофлоксацин), аминогликозидов (гентамицин, амикацин), производных фосфоновых кислот (фосфомицин) и нитрофуранов (нитрофурантоин) (Sigma-Aldrich, США) методом микроразведений в бульоне в соответствии с рекомендациями EUCAST Breakpoint tables v 13.0 (http://www.eucast.org). Категорию резистентности штамма определяли в соответствии с рекомендациями, предложенными в работе А.Р. Magiorakos и соавт. [4].
Методом ПЦР со специфичными праймерами в штаммах E. coli детектировали гены бета-лактамаз (blaTEM, blaCTX-M, blaOXA-48), интегразы классов 1 и 2 и их интегронные кассеты [11]; гены адгезинов (fimH, papGI, papGII, papGIII, sfaS, focG и afa/draBC), протектинов (ompT, traT, kpsMTII и kpsMTIII), сидерофоров (iroN, fyuA и iutA) и токсинов (hlyA, cnf1 и usp) [12]; маркерные гены биосинтеза специфичных О-антигенов [13], а также гены идентификации филогрупп по методу, предложенному в работе О. Clermont и соавт. [14]. Мультилокусное сиквенс-типирование штаммов E. coli проводили с помощью ПЦР-амплификации и секвенирования 7 генов «домашнего хозяйства» по схеме Achtman с последующим определением аллельного профиля на сайте Уорикского университета (http://enterobase.warwick.ac.uk/species/ecoli/allele_st_search) [15]. Последовательности ПЦР-продуктов секвенировали в ООО «СИНТОЛ» (Москва, Россия) и анализировали с помощью программ Chromas (http://technelysium.com.au/wp/chromas/) и Vector NTI 9 (Life Technologies, США).
Статистический анализ и графическую визуализацию экспериментальных данных проводили с помощью стандартных функций пакета Microsoft Office 2010 и программы SPSS Statistics 17.0.
В базе данных GenBank размещена полная последовательность генома штамма E. coli K369, код доступа JAHWEC000000000.
Результаты
Штаммы E. coli (n = 303) выделены в лечебных учреждениях России в 2004–2019 гг. из образцов мочи пациентов с диагнозами: «инфекция мочевыводящих путей без установленной локализации» (n = 258), «хронический цистит» (n = 26), «бессимптомная бактериурия» (n = 4), «острый пиелонефрит» (n = 4), «цистит» (n = 3), «хронический пиелонефрит» (n = 3), «гестационный пиелонефрит» (n = 2), «мочекаменная болезнь» (n = 2) и «гиперактивный мочевой пузырь» (n = 1).
Установлено, что в изученной коллекции E. coli резистентны к бета-лактамам 92% штаммов, фторхинолонам – 67%, аминогликозидам – 38%, нитрофуранам – 18% и фосфомицинам – 14% штаммов (рисунок, а).
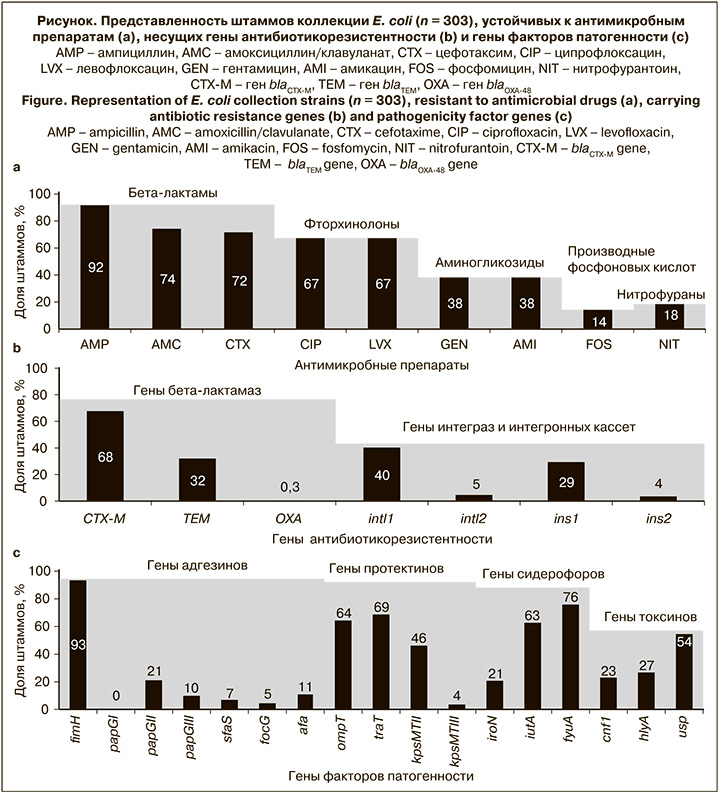
Полученные данные позволили отнести 4% штаммов коллекции к S-фенотипу, 51% – к R-фенотипу и 45% – к MDR-фенотипу, согласно рекомендациям А.Р. Magiorakos и соавт. [4]. В 77% штаммов коллекции детектированы один или несколько генов бета-лактамаз, а в 43% – ген интегразы класса 1 (рисунок, б). При этом в 39% штаммов найдены одновременно гены бета-лактамаз и интегразы. В 18% штаммов не выявлена ни одна из детектируемых генетических детерминант антибиотикорезистентности.
В исследованных штаммах E. coli выявлены 4 группы генов, ассоциированных у УПЭК с патогенностью (рисунок, в). В каждом штамме детектирован хотя бы один из генов патогенности: адгезин (94% штаммов), протектин (92%), сидерофор (88%) и токсин (57%). 77% изученных штаммов имели хотя бы один ген факторов патогенности из каждой группы: адгезинов, протектинов и сидерофоров.
В 197 из 303 штаммов выявлены генетические маркеры, ассоциированные с О-серологическими группами E. coli. Широко представлены маркеры серогрупп O25 (n = 112), O2 (n = 17), O8 (n = 12), O6 (n = 9), O89 (n = 7), O15 (n = 6), O86 (n = 5), O75 (n = 4) и O9 (n = 4). Кроме того, выявлены маркеры серогрупп O4, O11, O17, O18, O22, O91, O100, O101, O102, O106, O115, O134 и O143 (у 1–3 штаммов каждый). Для 106 штаммов О-группы не идентифицированы с помощью использованного метода типирования.
Для 294 штаммов коллекции E. coli определена принадлежность к 8 филогенетическим группам: A, B1, B2, C, D, E, F и кладе I. Наиболее представлена филогруппа B2 (51% штаммов), менее – филогруппы A (17%), E (9%), B1 (8%), D (7%), F (3%), клада I (2%) и C (1%).
Для 61 штамма изученной коллекции были идентифицированы сиквенс-типы на основании анализа аллельного профиля 7 генов «домашнего хозяйства» по схеме Achtman [11]. Сиквенс-тип ST131 определен у 11 штаммов, ST69 и ST127 – у 5 штаммов каждый, ST73 – у 4, ST141 – у 3, ST38, ST58, ST405, ST457, ST1193, ST1196 и ST1858 – у 2 штаммов каждый, а ST12, ST14, ST46, ST93, ST165, ST167, ST297, ST501, ST540, ST569, ST617, ST744, ST1140, ST1429, ST1434, ST5958, ST9239, ST10102 и ST12358 – у 1 штамма каждый.
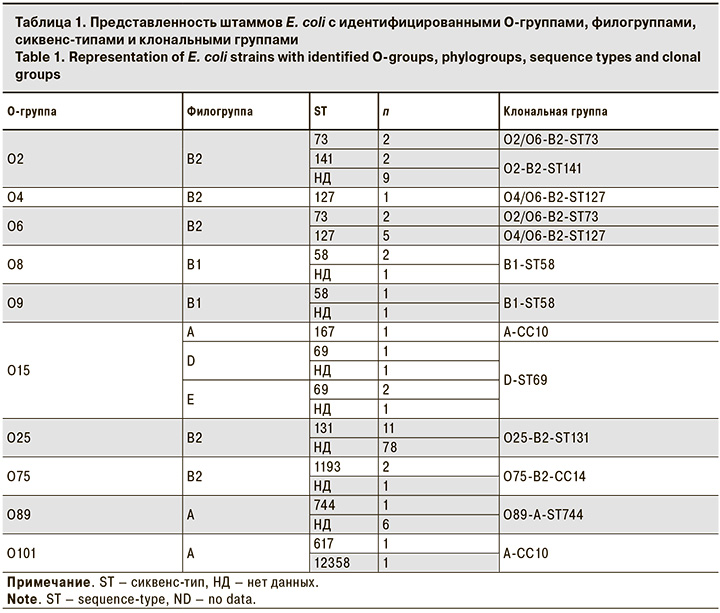
В ходе исследования на основании идентифицированных О-групп, филогрупп и сиквенс-типов для 180 штаммов коллекции определена принадлежность к 22 клональным группам E. coli, причем 133 штамма отнесены к 9 клональным группам, широко распространенным во всем мире: O25-B2-ST131, O2-B2-ST141, O89-A-ST744, O4/O6-B2-ST127, B1-ST58, D-ST69, O2/O6-B2-ST73, A-CC10 и O75-B2-CC14 (табл. 1).
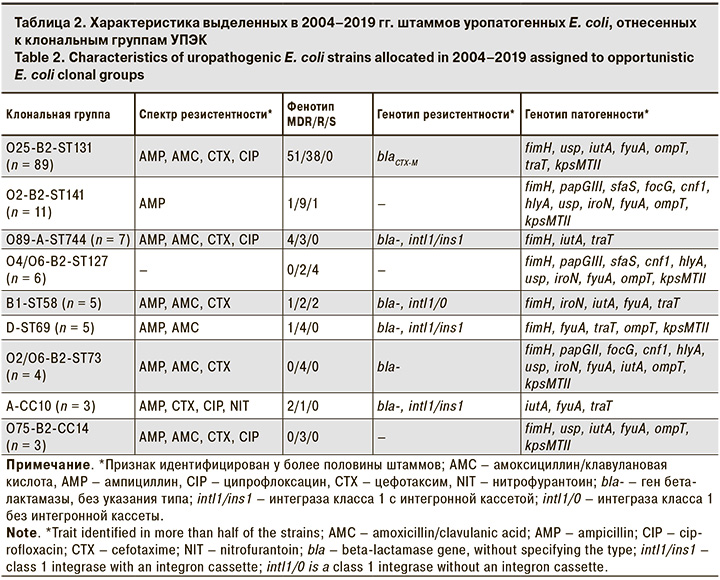
Штаммы нашей коллекции, отнесенные к самой распространенной в мире клональной группе O25-B2-ST131, обладали R- или MDR-фенотипом и несли по 5–10 генов вирулентности (табл. 2). В то же время штаммы клональных групп B1-ST58, O75-B2-CC14, D-ST69, A-CC10 и O89-A-ST744 обладали R- или MDR-фенотипом и несли 3–6 генов вирулентности.
Особенностью данного исследования является идентификация нового сиквенс-типа ST12358, характеризующегося аллельным профилем adk10, fumC11, gyrB4, icd8, mdh1153, purA13 и recA2 и отнесенного к известному клональному комплексу CC10. Штамм E. coli K369 с новым сиквенс-типом выделен в Первом МГМУ им. И.М. Сеченова в 2006 г. от пациента с ИМВП без установленной локализации.
Обсуждение
В ходе исследования выявлены фенотипические и молекулярно-генетические особенности штаммов УПЭК, выделенных в России в 2004–2019 гг. Показано, что доля штаммов с MDR-фенотипом в изученной нами коллекции составила 45%, что сопоставимо с долей таких штаммов из России, представленных в исследовании NoDARS в 2019 г. [16].
Серогруппы O25, O2, O8, O6, O89, O15, O86, O75 и O9 идентифицированы у 178 штаммов E. coli изученной коллекции, еще у 10 штаммов идентифицированы серогруппы O4, O11, O17, O18, O22, O102 и O134. При этом в базе данных EnteroBase (http://enterobase.warwick.ac.uk/species/index/ecoli) E.coli возбудители ИМВП этих серогрупп представлены более чем 5 штаммами каждый. Серогруппы O91, O100, O101, O106, O115 и O143, идентифицированные у 1–3 штаммов E. coli нашей коллекции, в базе данных EnteroBase как серогруппы E. coli возбудителей ИМВП не описаны.
Сиквенс-типы ST12, ST14, ST38, ST46, ST58, ST69, ST73, ST93, ST127, ST131, ST141, ST297, ST405, ST457, ST569, ST617, ST744, ST1193 и ST1196, идентифицированные у 1–11 штаммов E. coli нашей коллекции, найдены в базе данных EnteroBase у 2 и более E. coli возбудителей ИМВП каждый. При этом сиквенс-типы ST1858, ST165, ST501, ST540, ST1140, ST1429, ST1434 и ST5958, идентифицированные у 1–2 штаммов E. coli нашей коллекции, в базе данных EnteroBase как сиквенс-типы E. coli возбудителей ИМВП не описаны.
Наибольшее количество штаммов E. coli охарактеризованной нами коллекции (29%) отнесено к клональной группе O25-B2-ST131, которая является доминирующей группой УПЭК во всем мире. Полученные данные о высокой распространенности у этих штаммов устойчивости к бета-лактамам и ципрофлоксацину, MDR-фенотипа, а также встречаемости гена бета-лактамазы blaCTX-M и гена, кодирующего Usp-токсин, соответствуют опубликованным ранее данным [7–10]. Характеристика фенотипической резистентности, а также носительства генов резистентности и патогенности штаммов E. coli изученной коллекции, отнесенных к клональным группам O2-B2-ST141, B1-ST58, O2/O6-B2-ST73, D-ST69, A-CC10 и O75-B2-CC14, также согласуется с литературными данными [6–8, 17–21]. Интересно отметить, что в нашем исследовании все штаммы клональной группы O89-A-ST744 не несли ген hlyA, характерный для штаммов этой группы, описанной в работе Z. Hojabri и соавт. [9]. При этом все штаммы этой клональной группы в нашем исследовании были чувствительны ко всем использованным АМП, в то время как в работе M. Kubelová и соавт. [22] аналогичные штаммы описаны как множественно-резистентные. Отмеченные особенности предполагают наличие большей возможности выбора АМП в случае инфекции штаммами этой клональной группы.
Заключение
Проведенное ретроспективное исследование показало широкое распространение в России УПЭК-штаммов клональной группы O25-B2-ST131, а также выявило клональные группы O2-B2-ST141, O89-A-ST744, O4/O6-B2-ST127, B1-ST58, D-ST69, O2/O6-B2-ST73, A-CC10 и O75-B2-CC14. Полученные данные могут быть использованы для оценки текущей эпидемической ситуации по инфекциям мочевыводящей системы, прогноза ее развития в будущем, а также определения оптимальных направлений терапии.



