В структуре общей заболеваемости военнослужащих грипп и другие острые респираторные инфекции (ОРИ) составляют 35—50%. Особенно актуальна проблема ОРИ для воинских коллективов с наиболее высоким риском развития инфекций дыхательных путей, в частности вновь формируемых воинских частей, учебных центров, частей, участвующих в локальных военных конфликтах и миротворческих операциях. Пусковым механизмом активизации эпидемического процесса ОРИ в воинских коллективах
является их обновление. Доказательством этого служат связанные с призывами в Вооруженные
Силы Российской Федерации (ВС) выраженные подъемы в годовой динамике заболеваемости военнослужащих ОРИ.
Традиционные профилактические мероприятия, проводимые командованием, медицинской и другими службами, по оздоровлению условий труда и быта, укреплению общей резистентности военнослужащих до настоящего времени являются ведущими направлениями профилактики гриппа и других ОРИ в войсках. Однако устранение или ослабление отрицательного влияния этих и некоторых других социальных, санитарно-гигиенических, природных факторов на развитие эпидемического процесса не всегда представляется возможным. Кроме того, на фоне высокой заболеваемости ОРИ военнослужащих сохраняетсятенденциякростуихзаболеваемости внебольничными пневмониями (ВП). Особенно актуальна эта проблема в учебных соединениях и частях, заболеваемость ВП в которых в период приема молодого пополнения приобретает вспышечный характер, достигая 70—80% в структуре всей заболеваемости ВП в ВС.
Профилактика инфекций дыхательных путей предусматривает использование специфических и неспецифических медицинских средств. Специфическая вакцинопрофилактика существует только для гриппа. Однако в связи с тем, что удельный вес гриппа в структуре заболеваемости военнослужащих ОРИ составляет не более 1%, применение только противогриппозных вакцин в армейских коллективах вследствие превалирования инфекций, обусловленных возбудителями негриппозной этиологии, не позволяет решить проблему.
Значительные успехи в области иммунологии в последние десятилетия открыли перспективы для пересмотра прежних представлений о возможностях первичной профилактики ОРИ и создания соответствующих лекарственных средств. При этом основными требованиями к разрабатываемым препаратам являлись губительное воздействие на большинство респираторных вирусов в сочетании с нормализацией состояния иммунной системы (иммуномодулирующее действие) и как следствие с повышением неспецифической резистентности организма к респираторной вирусной инфекции при
отсутствии побочных эффектов. Оптимальным сочетанием вышеперечисленных свойств обладают препараты интерферона (ИФН).
Одним из современных препаратов этого ряда является виферон, гель — новая лекарственная
форма, разработанная ООО «ФЕРОН» (Россия). Имеющиеся научные данные характеризуют
виферон, гель как иммуномодулирующий препарат с выраженным противовирусным эффектом.
Основной компонент препарата — человеческий рекомбинантный интерферон альфа-2 оказывает выраженное противовирусное действие. Природный антиоксидант — витамин Е и его синергисты — бензойная и лимонная кислоты, метионин способствуют стабилизации клеточных мембран, обладают ранозаживляющим свойством. Гелевая основа обеспечивает пролонгацию воздействия препарата, а вспомогательные вещества — стабильность специфической активности и надлежащую микробиологическую чистоту препарата.
Применение препарата виферон, гель не требует предварительного иммунологического обследования. Лекарственная форма в виде геля обеспечивает простой, безопасный и безболезненный способ применения препарата.
В целях оптимизации профилактических мероприятий при гриппе и ОРИ среди военнослужащих проведена оценка эпидемиологической и иммунологической эффективности применения отечественного противовирусного препарата виферон, гель в организованных воинских коллективах учебного типа с высоким уровнем заболеваемости ОРИ.
Были изучены показатели заболеваемости ОРИ в основной и контрольной группах; проанализирована структура заболевших по этиологии, тяжести клинического течения заболевания, наличию осложнений и длительности трудопотерь; проведен мониторинг показателей местного, гуморального
и клеточного иммунитета при применении препарата виферон, гель; изучены возможные побочные
эффекты применения препарата.
Материалы и методы
Изучение эпидемиологической и иммунологической эффективности использования препарата виферон, гель проводилось в учебном центре, расположенном в Московской области. В оценке эффективности принимали участие курсанты учебного подразделения (практически здоровые молодые люди) в возрасте от 18 до 20 лет. Курсанты имели одинаковые условия размещения и службы. Исследуемый коллектив был сформирован во второй половине декабря 2009 г. из лиц, прибывших в основном из областей центральнойчастиРоссии —Ростовской,Калужской, Липецкой, Воронежской, Владимирской и Курской. Наблюдение проводилось в период с января по май 2010 г.
Под наблюдением находилось 383 курсанта, разделенных на 2 группы — основную (197 человек)
и контрольную (186 человек). Курсантам обеих групп в I декаде января 2010 г. была проведена
специфическая профилактика гриппа и пневмококковой инфекции вакцинами «Гриппол плюс»
и «Пневмо-23».
В основной группе курсантов для профилактики заболеваемости ОРИ был применен виферон, гель в соответствии с инструкцией по медицинскому применению препарата: 3 раза в день через 15—20 мин после приема пищи (после завтрака, обеда, ужина) в течение 3 нед. В контрольной группе курсантов (25 человек) виферон, гель не применялся.
С целью этиологической расшифровки ОРИ были проведены лабораторные исследования. У заболевших при госпитализации проводились молекулярно-биологические исследования (ПЦР) мазков
из носа и ротоглотки. Метод ПЦР применяли для определения возбудителей гриппа А, В, А H1N1-swine, микоплазмы пневмонии и хламидии пневмонии, аденовирусной инфекции, РС-инфекции (тест-системы ЗАО «АмплисенСенс», Россия). С помощью иммуноферментного анализа (ИФА) на 10—14-й день заболевания (тест-системы ЗАО «Вектор-Бест», Россия, «Nova Tec», Германия) определяли ранние антитела (IgМ) к возбудителям инфекционных заболеваний вирусной и бактериальной этиологии: гриппа А и В, парагриппа, цитомегаловирусной и РС-инфекции, аденовирусной инфекции, микоплазмы пневмонии и хламидии пневмонии.
У 50 курсантов до проведения профилактического курса препарата виферон, гель в основной группе и через 10 дней после окончания курса проводили иммунофенотипический анализ основных субпопуляций лимфоцитов периферической крови. Для иммунофенотипического исследования лимфоцитов использовали цельную венозную кровь, собранную в пробирки с К -ЭДТА. На двухлазерном проточном цитофлюориметре FACSCalibur (Becton Dickinson, США) с использованием 4-цветной панели антител MultiTEST IMK Kit (Becton Dickinson) исследовали процентное содержание основных субпопуляций лимфоцитов: Т-лимфоцитов (CD3+), Т-хелперов (CD3+CD4+), цитотоксических Т-лимфоцитов (ЦТЛ, CD3+CD8+), В-лимфоцитов (CD3-CD19+) и натуральных киллеров (CD3-CD16+56+).
Проведена оценка интерферонового статуса, а также определение уровня секреторного иммуноглобулина А (sIgA) в основной и контрольной группах курсантов по 25 человек в каждой
из групп (до начала и через день после окончания применения препарата). Определяли ИФН-α и γ
в сыворотке крови, а также уровни спонтанной и индуцированной продукции ИФН-α и γ клетками периферической крови в системе in vitro методом ИФА (тест-системы ЗАО «Вектор-Бест», Россия) до и на следующие сутки после окончания профилактического применения препарата.
С целью оценки иммунологической эффективности проводимых мероприятий было организовано определение уровня sIgA. Исследовали концентрацию sIgA в назальных пробах (экстракция мазка из носа в 1 мл физиологического раствора) методом ИФА (тест-системы ЗАО «Вектор-Бест», Россия) трижды за период наблюдения — до начала, на 12-й день и после окончания (на 32-й день).
Безопасность применения препарата виферон, гель учитывалась у всех военнослужащих, хотя бы раз получивших препарат. Критериями безопасности явились возникновение нежелательных явлений, серьезных нежелательных явлений, их связь с приемом препарата.
Репрезентативность выборочных групп и обеспечение их сопоставимости достигнуты случайным отбором групп военнослужащих с использованием таблицы равномерно распределенных случайных чисел и однородностью контингента, идентичностью условий его размещения, питания и военного труда. На каждую группу был составлен список лиц, включенных в исследование. Медицинское наблюдение за лицами основной и контрольной групп осуществлялось постоянно, в том числе в течение всего периода применения препарата. В период наблюдения учитывались все случаи заболеваний наблюдаемых военнослужащих ОРИ. Сведения о заболеваниях заносились в соответствующую графу списка основной или контрольной группы.
Напряженность эпидемического процесса в группах наблюдения оценивалась по показателю заболеваемости (I), рассчитываемому за период наблюдения (1 и 5 мес) на 100 человек по формуле:
I = (А·365·100)/N·Т, где:
А — число заболеваний;
N — численность группы наблюдения;
Т — длительность анализируемого периода.
Ущерб боевой подготовке оценивался по показателю неэффективности использования личного состава по причине болезни (R) по формуле:
R=I·t/Т (в% в день),
где:
I — показатель заболеваемости (в %);
t — показатель средней длительности одного
случая трудопотерь;
Т — длительность анализируемого периода в днях.
Оценка профилактической эффективности осуществлялась по частоте зарегистрированных случаев ОРИ в исследуемых группах в течение 5 мес наблюдения. Для оценки эпидемиологической эффективности также использованы индекс (ИЭ) и коэффициент (КЭ) эффективности:
где: ИЭ= p1/p2; КЭ = [(p1—p2)/p1]·100,
p — показатель заболеваемости в контрольной
группе;
p — показатель заболеваемости в группе лиц,
применявших виферон, гель.
При выполнении работы использованы общепринятые методы статистической обработки с определением средних величин, их доверительных интервалов и средних ошибок. Статистический анализ результатов проведен с использованием параметрических и непараметрических методов исследования.
Статистический анализ данных выполнялся с использованием пакета программ Statistica 6.1 (StatSoft, Inc., США). Описательная статистика количественных признаков представлена средними и ошибкой средней с отклонениями (в формате M±m; в случае нормальных распределений). Для сравнения несвязанных групп по количественным и порядковым признакам применялся тест Манна—Уитни, для сравнения связанных групп (анализа признаков в динамике) — тест Вилкоксона. Сравнение несвязанных групп по качественным признакам проводилось с использованием теста χ2 и точного критерия Фишера. При проверке гипотез результаты считались статистически значимыми при достигнутом уровне значимости p<0,05 [2].
Результаты и обсуждение
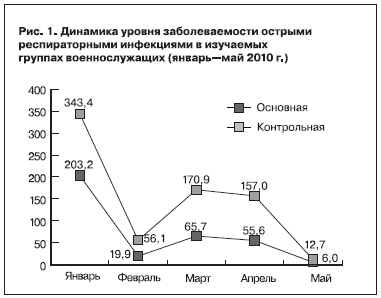
В течение периода наблюдения (январь — май 2010 г.) в исследуемых группах было зарегистрировано 168 случаев заболеваний ОРИ. Показатель заболеваемости за указанный период наблюдения составил 106,0 на 100 человек (табл. 1). Показатели помесячной заболеваемости ОРИ колебались от 6,0 до 203,2 на 100 человек в основной группе и от 12,7 до 343,4 на 100 человек в контрольной группе. Пик заболеваемости в обеих группах наблюдался в январе 2010 г. (см. табл. 1, рис. 1). При анализе заболеваемости ОРИ в динамике было установлено, что в основной группе
Таблица 1. Динамика уровня помесячной заболеваемости ОРИ и показателей
профилактической эффективности применения препарата виферон, гель в целях профилактики ОРИ
в изучаемых группах военнослужащих, январь—май 2010 г.
Выраженные различия обнаружены в структуре клинических проявлений ОРИ в наблюдаемых группах: в основной группе в 89,7% заболеваний имело место легкое клиническое течение, а случаев тяжелого клинического течения не отмечалось вовсе. В контрольной группе легкое клиническое течение ОРИ наблюдалось лишь у ⅔ заболевших, средней тяжести и тяжелое — в ⅓ случаев (табл. 2).
Таблица 2. Структура заболеваемости ОРИ по тяжести клинического течения
в исследуемых группах военнослужащих.
Были установлены существенные различия в средней длительности случая трудопотерь у больных ОРИ основной и контрольной групп в зависимости от тяжести клинического течения заболевания. Средняя длительность случая трудопотерь в контрольной группе колебалась от 5,7 до 9,3 дня в зависимости от тяжести клинического течения заболевания, в то время как в основной группе эти колебания составили от 4,5 до 6 дней. При сопоставимой численности групп наблюдения (197 и 186 человек) количество дней трудопотерь в связи с заболеванием ОРИ в контрольной группе превысило аналогичный показатель в основной группе в 2,5 раза. Показатели неэффективности использования
личного состава свидетельствуют о том, что ежедневно на протяжении анализируемого периода
(январь—май) в контрольной группе из каждых 100 человек не участвовали в боевой подготовке
по причине ОРИ в 2,7 раза больше военнослужащих, чем в основной группе (табл. 3).
Таблица 3. Длительность трудопотерь при заболеваемости ОРИ в изучаемых группах
военнослужащих и показатели неэффективности использования личного состава по причине ОРИ (R).
Таким образом, применение виферона, гель способствовало снижению показателя заболеваемости ОРИ в наблюдаемом воинском коллективе в 2 раза. Доля военнослужащих в основной группе, защищенных от ОРИ, составила 50,2% (см. табл. 1). Положительный профилактический эффект применения препарата виферон, гель в отношении ОРИ в основной группе был наиболее выражен в феврале 2010 г., т.е. через месяц после начала применения, и сохранялся на протяжении всего периода наблюдения.
При анализе этиологии установлено, что наиболее часто ОРИ среди курсантов вызывали возбудители аденовирусной инфекции (31,7%). Одновременно с аденовирусной инфекцией в коллективе определялись антитела к цитомегаловирусу, микоплазмам пневмонии, парагриппу (табл. 4, 5).
Таблица 4. Результаты серологических исследований сывороток от больных ОРИ на наличие ранних антител (IgМ) к возбудителям ОРИ.
Таблица 5. Результаты молекулярно-биологических исследований мазков из полости носа и ротоглотки от заболевших ОРИ военнослужащих на возбудители ОРИ.
Анализ частоты присоединения соматической и/или инфекционной патологии у больных ОРИ в исследуемых группах показал, что в 30,3% случаев имело место присоединение вторичной патологии. В структуре вторичных осложнений наиболее часто встречались ВП (23,2%) и бронхиты (7,1%). Применение препарата виферон, гель в основной группе способствовало уменьшению осложненных форм ВП и бронхитов в 2,4 и 2,1 раза (p<0,05) соответственно по сравнению с группой контроля. Показатели защищенности составили соответственно 58 и 52,8% (табл. 6).
Таблица 6. Частота присоединения вторичных осложнений среди военнослужащих,
заболевших ОРИ (январь—май 2010 г.).
Для оценки иммунологической эффективности проводимых мероприятий определяли уровень
sIgA и изучали иммунный и интерфероновый статус курсантов. Для скрининга состояния системы клеточного иммунитета и интерферонового статуса провели анализ показателей до начала исследования у 50 человек (13% от общего количества участников). При оценке интерферонового статуса до начала применения препарата виферон, гель было выявлено следующее: у 10 (20%) человек состояние системы интерферона соответствовало норме, в сыворотке отсутствовал ИФН-ά, спонтанной продукции его не наблюдалось и сохранялась способность лейкоцитов продуцировать ИФН-ά после индукции (299,46±105,30 пкг/мл). У 40 (80%) человек выявлено отклонение от нормы в продукции ИФН-ά клетками периферической крови, которое выражалось в значительном снижении способности продуцировать ИФН-ά (менее 50 пкг/мл), в этой же группе ИФН-ά обнаружен в сыворотке крови (43,82±4,31 пкг/мл) и отмечена спонтанная продукция ИФН-ά лейкоцитами периферической
крови (35,04±9,19 пкг/мл), что превышает значения нормы, в то время как продукция ИФН-γ
была близка к общепринятым нормам (табл. 7). Выявленные нарушения показателей интерферонового статуса у военнослужащих на этапе формирования воинских коллективов более всего указывают на угнетение системы интерферона под воздействием стрессорных факторов. По данным литературы, существует определенная взаимосвязь между степенью стрессорного воздействия и выработкой ИФН-α, которая выражается снижением продукции ИФН-α клетками периферической крови, вплоть до ее отсутствия на фоне стресса [3—6].
Таблица 7. Динамика продукции ИФН-ά и ИФН-γ (в пкг/мл) в наблюдаемых группах военнослужащих.
Таблица 8. Динамика основных субпопуляций лимфоцитов (в %) периферической крови
у наблюдаемых групп военнослужащих (М±m).
При исследовании основных субпопуляций лимфоцитов периферической крови у военнослужащих до начала применения препарата между двумя группами исследованных статистически значимых различий показателей клеточного иммунитета не обнаружено (табл. 8). При сравнении с нормальными показателями здоровых взрослых молодых людей можно отметить, что в обеих исследованных группах военнослужащих содержание натуральных киллеров от общего числа лимфоцитов находится на нижней границе нормы (7,28% в основной группе и 8,52% в контрольной группе по сравнению
с нормой 13±5%), что свидетельствует об исходной сниженной резистентности иммунитета обследованных к вирусной инфекции.
Через 10 дней после окончания курса в основной группе снова провели оценку показателей
клеточного иммунитета в обеих группах военнослужащих. При этом в контрольной группе
значимых различий по сравнению с исходными значениями показателей клеточного иммунитета не обнаружено. В то же время в группе военнослужащих, прошедших профилактический курс виферонотерапии, через 10 дней после окончания курса наблюдалось значимое увеличение
доли натуральных киллеров (11,42 против 7,28% исходно),атакжепропорциональноеувеличению
доли натуральных киллеров относительное снижение доли Т-лимфоцитов (74,55 против 79,38%
исходно), главным образом за счет Т-хелперов (43,06 против 48,96%). Относительного снижения
доли цитотоксических Т-лимфоцитов не наблюдалось, и поддержание их количества на достаточном уровне обеспечило развитие адекватного цитотоксического ответа организма на вирусную инфекцию.
Таким образом, профилактический эффект применения препарата виферон, гель у исследованной группы военнослужащих обусловлен нормализацией основных показателей клеточного иммунитета, в частности увеличением доли натуральных киллеров, которые играют ключевую роль в эффективной защите организма от вирусных, в том числе респираторных, инфекций [7—9].
У этих же военнослужащих проводили оценку иммунного и интерферонового статуса в динамике — до начала и на следующий день после окончания применения препарата (см. табл. 7, 8). При анализе каждой из наблюдаемых групп нами выявлены некоторые различия стартовых значений интерферонового статуса. Военнослужащие, условно здоровые молодые люди, без каких-либо
признаков острых и хронических заболеваний имели различные патологические варианты
состояния интерфероногенеза. Так, в основной группе до применения препарата показатели
интерферонового статуса не соответствовали нормальным у всех обследованных: у 64% ИФН-α
не определялся в сыворотке крови, не было спонтанной продукции и способность клеток периферической крови вырабатывать ИФН-α была крайне низкой, у 36% военнослужащих, напротив, выявлялся высокий уровень ИФН-α в сыворотке и спонтанной продукции, низкая индуцированная продукция ИФН-α клетками крови.
После применения препарата виферон, гель у 100% наблюдаемых основной группы способность клеток к продукции ИФН-α в ответ на индукцию восстановилась, небольшое количество (в пределах нормы) спонтанного ИФН-α и в сыворотке крови объясняется наличием ИФН-α в самом препарате.
В то же время в контрольной группе происходило истощение интерфероногенеза: у 10 (40%) военнослужащих стартовые значения интерферонового статуса соответствовали норме: сывороточный и спонтанный ИФН-α не определялись и способность лимфоцитов продуцировать
ИФН-ά была на уровне 368,86±171,25 пкг/мл, через 3 нед у тех же наблюдаемых отсутствовал ИФН-α в сыворотке и не было спонтанной продукции ИФН-α клетками периферической крови, а индуцированная продукция снижалась, вплоть до ее полного отсутствия. У 15 (60%) наблюдаемых контрольной группы в начале исследования выявлено напряжение интерфероногенеза: высокий уровень сывороточного и спонтанного ИФН-α и невысокая продукция ИФН-α клетками периферической крови после стимуляции в системе in vitro. Без проведения профилактических мероприятий у данной группы военнослужащих также происходило истощение интерфероногенеза, которое выражалось в неспособности лимфоцитов вырабатывать ИФН-α в ответ на стимуляцию. На этом фоне существенно возрастает возможность инфицирования и заболевания ОРИ, развития осложненных форм в виде бронхитов и ВП, обострения хронических заболеваний.
Таблица 9. Динамика изменения продукции sIgA (в мг/мл) в изучаемых группах военнослужащих.
При оценке показателей исходного уровня sIgA в назальных пробах достоверно значимых различий между группами не выявлено (1-я точка) (табл. 9). После начала применения препарата средний уровень sIgA в основной группе повысился с 16,53±3,38 до 26,70±3,07 мг/л (различия с контрольной группой статистически достоверны; p‹0,05) (2-я точка). В контрольной группе продукция секреторного sIgA была ниже, чем в основной. Наиболее значимым было различие на 32-й день исследования (3-я точка), когда уровень продукции sIgA в контрольной группе был ниже, чем в основной, практически в 3 раза. Это объясняется влиянием ИФН-α на гуморальный иммунитет, в частности на увеличение и пролонгацию секреции sIgA эпителиоцитами. Иммуноглобулины этого класса предотвращают инфицирование патогенами, проникающими через слизистые оболочки [10—11]. Таким образом, применение виферон, геля обеспечило выраженный протективный эффект в отношении заболеваемости ОРИ в основной группе курсантов (рис. 2, см. на вклейке).
В период исследования у лиц, получавших препарат виферон, гель, не выявлено каких-либо нежелательных, в том числе и серьезных, явлений.
Выводы
1. Препарат виферон, гель обладает выраженными протективными свойствами в отношении ОРИ.
2. Использование препарата виферон, гель с профилактической целью позволяет существенно снизить показатель заболеваемости ОРИ стройств в организованных воинских коллективах (коэффициент эпидемиологической эффективности препарата составляет 50,2%, индекс эффективности — 2,0). При этом у военнослужащих, применяющих данный препарат, также отмечается снижение заболеваемости бронхитами в 2,1 раза, ВП в 2,4 раза.
3. Применение местной формы интерферона человеческого рекомбинантного альфа-2 в виде
препарата виферон, гель приводит к статистически значимому повышению (р<0,05) уровня секреторного IgA в носовых секретах (основного фактора защиты во входных воротах инфекции) по сравнению с контрольной группой, что обусловливает его протективный противовирусный эффект.
4. Применение препарата виферон, гель приводит к иммуномодулирующему действию на систему интерферона, что подтверждается статистически значимым повышением индуцированной
продукции ИФН-α и -γ клетками периферической крови в системе in vitro, а также на состояние
клеточного гуморального иммунитета, способствуя повышению общей неспецифической резистентности организма военнослужащих к ОРИ.
5. Препарат хорошо переносится, не дает побочных эффектов и не вызывает аллергических реакций.
6. Препарат виферон, гель рекомендуется для широкого применения в целях профилактики
ОРИ и их осложнений в организованных коллективах военнослужащих. Наиболее целесообразно применение данного препарата с профилактической целью в период формирования воинских коллективов.



