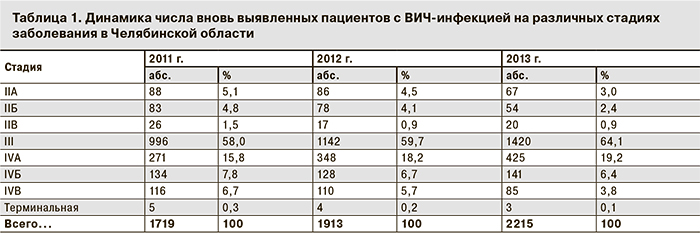
Челябинская область занимает 10-е место в России по числу ВИЧ-инфицированных жителей, при этом общее число пациентов с ВИЧ-инфекцией, требующих постоянного наблюдения, составляет более 25 000. В настоящее время в области отмечается тенденция к увеличению числа вновь выявленных пациентов с ВИЧ-инфекцией на продвинутых стадиях болезни с различными клиническими проявлениями вторичных заболеваний, что требует незамедлительного начала интегрированной антиретровирусной терапии (АРВТ) ВИЧ и оппортунистических инфекций (табл. 1). При выборе схем АРВТ первой линии у данной категории пациентов следует принимать во внимание множество факторов: сопутствующие заболевания и оппортунистические инфекции; исходно низкий уровень иммунного статуса пациентов; психоэмоциональное состояние и, как следствие, потенциальную неприверженность, которая напрямую зависит от удобства приема АРВТ (количества таблеток и частоты их приема в течение суток, связи с приемом пищи или жидкости); возможные нежелательные реакции (НР). Своевременная коррекция этих факторов позволит быстро достичь полного подавления вирусной нагрузки (ВН) и восстановить пул CD4+-лимфоцитов при наименьших проявлениях НР, а также сформировать приверженность, что особенно важно в начале лечения.
В современных международных рекомендациях по лечению ВИЧ-инфекции выбор препаратов для начала терапии приблизительно одинаков, при этом в качестве предпочтительного третьего компонента отмечается равнозначность выбора как ненуклеозидного ингибитора обратной транскриптазы (ННИОТ), так и усиленного ритонавиром ингибитора протеазы (ИП). В большинстве проведенных ранее исследований показана сравнимая вирусологическая эффективность режимов с ННИОТ и ИП [1–3]. Что касается иммунологической эффективности, то в ряде исследований продемонстрирован бóльший прирост CD4+-лимфоцитов в группе пациентов, получавших ИП [2, 4]. Кроме того, в случаях неудачи лечения отмечается существенно меньшее количество мутаций, вызывающих устойчивость ВИЧ к антиретровирусным препаратам, при применении ИП по сравнению с ННИОТ. Этот факт, безусловно, свидетельствует о больших возможностях выбора препаратов для продолжения лечения при применении ИП в схемах АРВТ первой линии [4]. С точки зрения безопасности для этих классов препаратов, а также для отдельных их представителей характерен различный профиль возможных НР, которые следует учитывать при выборе схем для разных категорий пациентов.
Еще в 2006 г. рекомендации Департамента здравоохранения США (DHHS) в качестве предпочтительного начального режима с ИП включали только препарат лопинавир/ритонавир (LPV/r). В процессе совершенствования АРВТ данный класс пополнился новыми представителями. Не меньшая эффективность ИП фосампренавира (FPV), саквинавира (SQV), атазанавира (ATV) и дарунавира (DRV) по сравнению с LPV/r была продемонстрирована в нескольких крупных многоцентровых рандомизированных исследованиях (KLEAN [5], GEMINI [6], CASTLE [7] и ARTEMIS [8] соответственно). В результате в 2008 г. во многие рекомендации они были включены в качестве препаратов выбора для начала АРВТ.
Исследование KLEAN послужило основой для принятия решения о включении ИП FPV (телзир; компания «ViiV Healthcare», Великобритания) в схемы АРВТ первой линии. В настоящее время получены результаты 144 нед. лечения в рамках данного протокола, которые свидетельствуют о сравнимой длительной эффективности и сопоставимом профиле безопасности схем, включающих FPV/r 700/100мг и LPV/r 400/100 2 раза в сутки в комбинации с 2 НИОТ (абакавир/ламивудин) [5]. Помимо исследования KLEAN сравнение данных схем проводили в наблюдательном исследовании итальянские авторы [9]. Согласно результатам их наблюдений на протяжении 18 мес., схемы АРВТ, включающие FPV/r и LPV/r, были сопоставимы по эффективности, однако при применении FPV/r был продемонстрирован более благоприятный профиль безопасности, в частности диарея развивалась реже, а процент прерывания терапии по этой причине был ниже по сравнению с LPV/r (р = 0,006 и 0,008 соответственно).
В ряде исследований продемонстрировано, что однократный (в сутки) прием FPV в дозе 1400 мг может быть усилен ритонавиром в уменьшенной дозе (100 мг) без ущерба для эффективности [10, 11]. В исследовании C. Hicks и соавт. [10] отмечена даже более высокая вирусологическая эффективность в группе пациентов, получавших FPV/r 1400/100 мг 1 раз в сутки, по сравнению с пациентами, получавшими FPV/r в дозе 1400/200 мг 1 раз в сутки, при оценке методом ITT (доля пациентов с РНК ВИЧ-1 < 400 копий/мл – 78 и 53% соответственно; p < 0,006) после 96 нед. лечения, что было обусловлено лучшей приверженностью пациентов к терапии, связанной с уменьшением количества таблеток и улучшением переносимости (снижение частоты и степени тяжести диареи, снижение числа ранних отказов от АРВТ, более благоприятный липидный профиль). В исследовании ALERT [12] сравнивали результаты однократного (в сутки) режима приема FPV/r 1400/100 мг и схемы с ATV/r (300/100 мг 1 раз в сутки) в комбинации с тенофовиром/эмтрицитабином (TDF/FTC) у 106 пациентов, ранее не получавших АРВТ. Результаты свидетельствуют о сравнимой эффективности схем терапии даже у пациентов с исходной ВН ≥100 000 копий/мл (доля пациентов с РНК ВИЧ-1 < 400 копий/мл к 48-й неделе по результатам ITT-анализа: MD=F – 79 и 79%; Obs – 95 и 90% соответственно). В исследовании была отмечена меньшая частота НР 2–4-й степени на фоне приема FPV/r из-за отсутствия повышения уровня сывороточного билирубина (15 и 57% соответственно). Содержание липидов изменялось одинаково в обеих группах [12].
В настоящее время ведущие международные и российские рекомендации по лечению ВИЧ-инфекции [Европейского клинического общества СПИДа (EACS); Министерства здравоохранения и социального обеспечения США (DHHS); Национального научного общества инфекционистов России; Национальные клинические рекомендации по диагностике и лечению ВИЧ-инфекции у взрослых (Россия)] рассматривают применение FPV/r в комбинации с препаратами класса НИОТ в АРВТ первой линии в качестве предпочтительной либо альтернативной схемы [13–16].
В доступной нам литературе недостаточно сведений об опыте применения FPV у российских пациентов, поэтому целью нашего анализа является оценка эффективности и экономической целесообразности применения схем АРВТ первой линии, включающих FPV/r в дозе 1400/100 мг 1 раз в сутки, у пациентов без опыта терапии.
Материалы и методы
На базе Челябинского областного центра по профилактике и борьбе со СПИД и инфекционными заболеваниями был проведен ретроспективный анализ данных 43 амбулаторных пациентов с ВИЧ-инфекцией, получающих с 2012 г. схемы АРВТ первой линии, в состав которых был включен FPV/r в дозе 1400/100 мг 1 раз в сутки.
Конечные точки исследования. Первичная конечная точка – определение доли пациентов с ВН < 150 копий/мл на 12-й, 24-й, 48-й и 72-й неделе исследования. Вторичные конечные точки – изменения уровня СD4-лимфоцитов по сравнению с исходным на 12-й, 24-й, 48-й и 72-й неделе; расчет и оценка прямых затрат на исследуемые схемы терапии ВИЧ-инфекции.
Полученные результаты были обработаны статистически в программе Statistiсa 8 («StatSoft Inc.», США) непараметрическими методами. Для парных сравнений использовали критерий Вилкоксона, для множественных – ранговый дисперсионный анализ по Фридману. Различия показателей признавали статистически достоверными при p < 0,05. Данные описывали с использованием медианы и квартилей
(Me [Q25; Q75]). Расчет темпа прироста CD4-лимфоцитов проводили по общепринятой формуле [17]:

Результаты и обсуждение
Общая характеристика пациентов
В 2012 г. схемы АРВТ с FPV/r начали получать 76 пациентов, из них 71 (93%) – в первой линии терапии. За период наблюдения 5 (6,5%) человек самостоятельно отказались от лечения в связи с социальными показаниями (активное употребление наркотических веществ и алкоголизм); у 7 (19,4%) из 36 пациентов, получавших FPV/r в комбинации с фиксированной комбинацией доз (ФКД) зидовудина/ламивудина (ZDV/3TC), в связи с развитием анемии была произведена замена НИОТ зидовудина (ZDV) на абакавир (ABC). Был зарегистрирован 1 случай смерти на 2-й неделе терапии в связи с поздним началом лечения и распространенными вторичными заболеваниями (токсоплазмоз головного мозга, генерализованная ЦМВ-инфекция). В целом из числа пациентов (п = 71), начавших принимать FPV/r в АРВТ первой линии, 65 получали назначенный режим на протяжении 18 мес.
Детально были проанализированы данные 43 пациентов, принимающих FPV/r в АРВТ первой линии не менее 18 мес. Все пациенты получали препарат в комбинации с 2 НИОТ. В зависимости от схемы АРВТ пациенты были распределены в 3 группы. 1-ю группу составили 15 пациентов, получавших АРВТ на основе ФКД ZDV/3TC 2 раза в сутки и FPV/r 1400/100 мг 1 раз в сутки. Во 2-ю группу были включены 15 пациентов, получавших в виде монокомпонентов АВС (зиаген; компания «ViiV Healthcare», Великобритания) + 3ТС (ламивудин-3ТС; компания ООО «Технология лекарств», Россия) 2 раза в сутки и FPV/r 1400/100 мг 1 раз в сутки. В 3-ю группу были включены 13 пациентов, получавших ФКД ABC/3TC1 (кивекса; компания «ViiV Healthcare», Великобритания) и FPV/r 1400/100 мг 1 раз в сутки. Группы были сопоставимы по полу, возрасту, исходному уровню ВН и продолжительности заболевания до начала АРВТ. В 3-й группе медиана исходного уровня CD4+-лимфоцитов была ниже, чем в других группах, однако статистически это не подтвердилось.
Социальный статус больных был достаточно низкий, только 25 (58%) из них имели постоянную работу. У 27 (63%) пациентов инфицирование ВИЧ произошло при внутривенном употреблении наркотических средств, при этом большинство из них (85%) оказались в 1-й группе. До назначения АРВТ у всех пациентов была ВИЧ-инфекция в стадии 4Б–4В с соответствующими вторичными заболеваниями. Анализ данных амбулаторных карт показал, что при соблюдении режима АРВТ ни у одного пациента не было зарегистрировано прогрессирования ВИЧ-инфекции или развития НР в ответ на проводимую терапию.
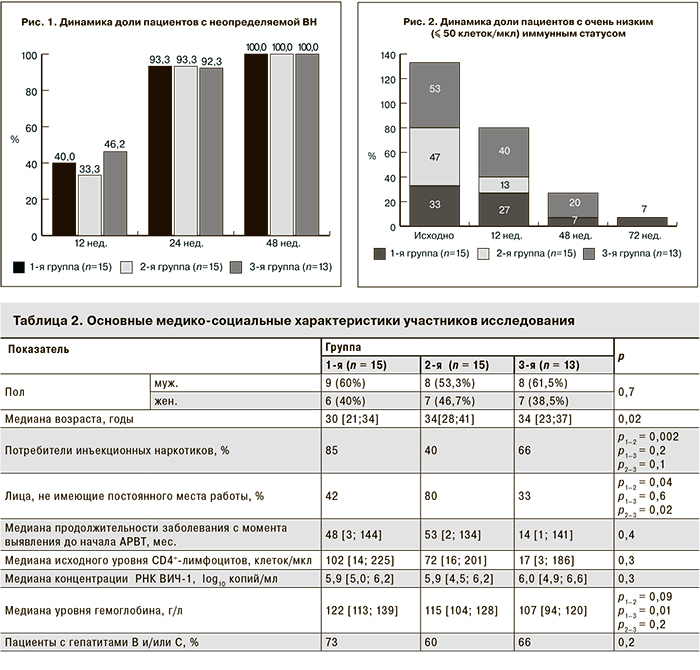
Исходные клинико-социальные характеристики пациентов представлены в табл. 2.
Результаты и обсуждение
Оценка эффективности АРВТ
 В ходе анализа неопределяемый уровень ВН у подавляющего большинства пациентов во всех исследуемых группах был достигнут уже к 24-й неделе терапии (рис. 1). Наблюдалась положительная динамика прироста доли пациентов, достигших ВН < 150 копий/мл, в течение всего периода АРВТ с FPV/r, независимо от назначенной нуклеозидной основы, и уже к 48-й неделе у 100% пациентов была достигнута неопределяемая ВН.
В ходе анализа неопределяемый уровень ВН у подавляющего большинства пациентов во всех исследуемых группах был достигнут уже к 24-й неделе терапии (рис. 1). Наблюдалась положительная динамика прироста доли пациентов, достигших ВН < 150 копий/мл, в течение всего периода АРВТ с FPV/r, независимо от назначенной нуклеозидной основы, и уже к 48-й неделе у 100% пациентов была достигнута неопределяемая ВН.
При оценке иммунного статуса пациентов отмечено достаточно большое число больных с исходно очень низким (≤ 50 клеток/мкл) уровнем CD4-лимфоцитов во всех группах, а в 3-й группе таких пациентов было большинство (53%). В динамике доля этих пациентов во всех группах снижалась (рис. 2). Отмечено, что у пациентов 1-й группы, получавших FPV/r в комбинации с ФКД ZDV/3TC, снижение было более медленным по сравнению с пациентами, получавшими схемы, включающие АВС. Через 72 нед. АРВТ пациенты с очень низким иммунным статусом остались только в 1-й группе, что подтверждает преимущества схем, включающих АВС, с точки зрения иммунологической эффективности [18].
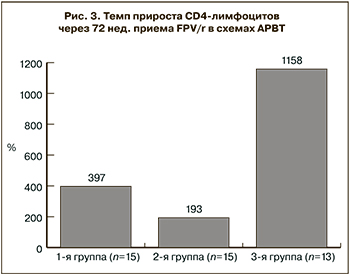
Следует отметить, что исходный уровень CD4-лимфоцитов у пациентов 3-й группы был ниже, чем у пациентов 1-й и 2-й групп, однако к 72-й неделе лечения показатель иммунного ответа во всех группах был сопоставим (табл. 3).
В течение 72 нед. терапии прирост CD4-лимфоцитов наблюдался во всех группах, однако максимальным (+1158%) он оказался у пациентов 3-й группы (рис. 3).
Полученные нами данные подтвердили результаты исследований, свидетельствующие о высокой вирусологической эффективности режимов с однократным (в сутки) приемом FPV/r [10–12]. Отмечалась лучшая иммунологическая эффективность схем с FPV/r, включающих в качестве нуклеозидной основы АВС, по сравнению со схемами, включающими ZDV, о чем свидетельствовало более быстрое снижение доли пациентов с уровнем CD4-лимфоцитов ≤ 50 клеток/мкл и отсутствие таких пациентов через 72 нед. АРВТ во 2-й и 3-й группах. Кроме того, результаты наглядно показали преимущества схемы ФКД АВС/3ТС + FPV/r у пациентов с исходно низкими показателями иммунного статуса, так как темп прироста CD4-лимфоцитов в этой группе был в 3 раз выше, чем в 1-й группе и в 6 раза выше, чем во второй. Возможно, несколько более низкие показатели иммунологической эффективности у пациентов 1-й группы были обусловлены низким уровнем приверженности к терапии из-за большого числа (85%) потребителей инъекционных наркотиков среди них.
Оценка и анализ прямых затрат на исследуемые режимы АРВТ
Прямые затраты на проведение АРВТ рассчитывали на основании стоимости лекарственных препаратов по данным электронных аукционов (http://www.zakupki.gov.ru), проведенных в 2012 г. (на момент начала исследования) в рамках реализации приоритетного национального проекта в сфере здравоохранения, раздел «Профилактика ВИЧ-инфекции, гепатитов В и С, выявление и лечение больных ВИЧ», так как стоимость препаратов в государственном реестре цен на лекарственные препараты, входящие в список жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП), в ряде случаев не отражает их истинной цены в регионе (табл. 4).
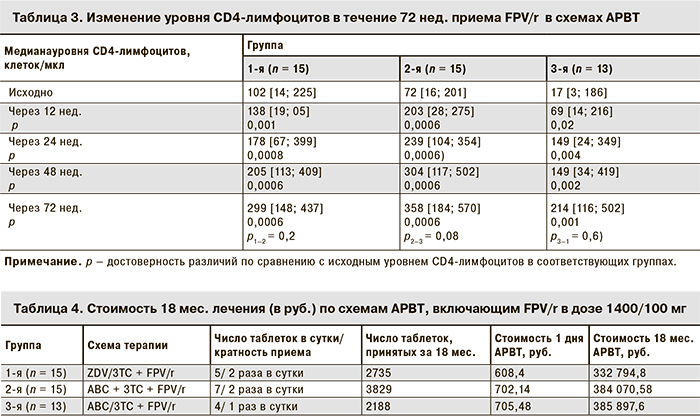
Как следует из данных, приведенных в табл. 4, среди схем АРВТ, включающих FPV/r в дозе 1400/100 мг в качестве третьего компонента, наименее экономически затратной была ZDV/3TC + FPV/r. Схемы, содержание в качестве нуклеозидной основы ФКД ABC/3TC и монокомпоненты ABC + 3TC, по стоимости значительно не различались. Однако следует отметить, что пациентам с исходно низким (< 200 клеток/мкл) иммунным статусом назначать ZDV в схеме АРВТ нецелесообразно, так как они входят в группу риска по развитию анемии и часто имеют исходно низкий уровень гемоглобина, соответственно при назначении ZDV степень анемии может усугубиться [19]. Например, в нашем исследовании 6 (13,9%) пациентам с исходно низким уровнем гемоглобина схема, содержащая ФКД ZDV/3TC, изначально не могла быть назначена.
Ретроспективный анализ данных 43 ВИЧ-инфицированных амбулаторных пациентов на протяжении 72 нед. показал высокую эффективность однократного (в сутки) режима приема FPV/r в дозе 1400/100 мг в комбинации с разной нуклеозидной основой в АРВТ первой линии. Более высокую иммунологическую эффективность продемонстрировали схемы, включающие FPV/r в комбинации с нуклеозидной основой, содержащей АВС, а максимальный темп прироста CD4-лимфоцитов (+1158%) через 72 нед. АРВТ был отмечен в группе пациентов, получавших FPV/r в комбинации с ФКД ABC/3TC. Возможно, это связано не только со свойствами самих препаратов, но и с удобством их приема и, следовательно, лучшей приверженностью к терапии.
Схема АРВТ ФКД ABC/3TC + FPV/r сопоставима по стоимости со схемой ABC + 3TC + FPV/r и более экономически затратна по сравнению с ZDV/3TC (ФКД) + FPV/r, однако в силу ряда преимуществ (прием 1 раз в сутки, минимальное число таблеток, благоприятный профиль безопасности) является оптимальным выбором АРВТ первой линии для пациентов, так как обеспечивает долгосрочную эффективность и безопасность лечения.


