Рак шейки матки (РШМ) является четвертым по частоте встречаемости и смертности видом рака в мире среди женщин: в 2020 г. зарегистрировано 604 000 новых случаев и более 340 000 смертельных исходов от этой нозологии, что составляет 7,7% всех смертей, связанных с опухолями [1]. Число случаев РШМ в России за 10 лет (2009–2019 гг.) увеличилось на 22% (с 14 000 до 17 000), что демонстрирует социальную значимость данного заболевания. На группу женщин социально активного и репродуктивного возраста 30–44 лет приходится 32,4% случаев РШМ [2].
Согласно статистике по оказанию онкологической помощи населению России, общепринятые механизмы профилактики предраковых заболеваний шейки матки работают недостаточно эффективно: нет всеобщей вакцинации, женщины не информированы о необходимости и возможности цитологического исследования, часто отсутствуют информированность населения и мотивация к регулярному обследованию. В связи с этим смертность от РШМ практически не снижается [2].
Доказанным этиологическим агентом РШМ является вирус папилломы человека (ВПЧ). Показано, что связь с ВПЧ и РШМ выше, чем связь между курением и раком легкого [3]. При этом у ВПЧ-инфицированных женщин частота РШМ составляет всего 0,015%, что позволяет предполагать наличие генетической предрасположенности [4]. К факторам генетической предрасположенности относятся различные вариации в последовательности ДНК: одиночные нуклеотидные замены, делеции, инсерции и структурные вариации. При этом подавляющее большинство изменений вносят однонуклеотидные полиморфизмы (ОНП) – нуклеотидные замены, встречающиеся чаще чем у 1% лиц в популяции [5].
Определение ОНП, ассоциированных с заболеваниями, позволяет охарактеризовать возможную наследственную предрасположенность к развитию патологических состояний в досимптоматический период для своевременного назначения диагностических или профилактических мероприятий [5].
Учитывая длительный бессимптомный период, половой путь передачи и поражение женщин репродуктивного возраста, прогнозирование развития РШМ является важной клинической задачей, особенно актуальной для женщин из групп риска, к которым, в том числе, относятся ВИЧ-инфицированные [6].
В данный момент в России существует проблема малого охвата профилактическим скринингом РШМ, так как существующий «оппортунистический скрининг» достигает не более 30%. Выявление групп риска скринингом является актуальной задачей для современного общества в эпидемиологическом контроле за РШМ [7]. Определение аллелей ОНП, ассоциированных с РШМ, и математические расчеты генетически обусловленных рисков смогут помочь в решении задачи оптимизации риск-ориентированного подхода в эпидемиологическом надзоре за РШМ с целью корректировки и своевременного назначения диагностических и профилактических мероприятий.
Традиционные методы прогнозирования риска развития заболеваний и патологических процессов – это регрессионный анализ, анализ временных рядов, деревья решений и экспоненциальное сглаживание [8]. При этом если зависимая переменная имеет 2 класса: «да» (наличие признака) или «нет» (отсутствие признака), совокупность методов сужается до регрессионного анализа, а именно бинарной-логистической регрессии, и дерева решений. Однако эти методы имеют несколько недостатков, например, регрессионный анализ имеет проблемы мультиколлинеарности, сложности выбора предикторов и ошибки в интерпретации коэффициента ответа [9]. Наиболее подходящее решение проблемы – использование машинного обучения и тестирование множества различных моделей с выбором оптимальной, то есть с наименьшим количеством ошибочных предсказаний. Для регрессионного анализа – это лассо-регрессия или гребневая регрессия, для метода дерева решений – случайные леса, Gradient Boosting Machine (GBM) и XGBoost [10], а также получившие популярность в эпидемиологических исследованиях нейронные сети [11].
Следует признать, что на сегодняшний момент недостаточно данных для выбора оптимального метода прогнозирования в эпидемиологических исследованиях с анализом генетических рисков, которые не обладают 100% пенетрантностью.
Таким образом, цель исследования – сравнение и выбор наиболее оптимального метода машинного обучения для прогнозирования развития РШМ у ВПЧ-инфицированных женщин с использованием данных о носительстве ряда генетических полиморфизмов.
Материалы и методы
Были исследованы образцы из базы данных «Распространенность вируса папилломы человека различного канцерогенного риска среди населения Московского региона»1. Пробы ДНК 247 ВПЧ-инфицированных женщин экстрагировали из соскобов со слизистой оболочки цервикального канала (экзоцервикс и эндоцервикс). Образцы предварительно тестировали на наличие ДНК ВПЧ 14 онкогенных типов (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) методом полимеразной цепной реакции в режиме реального времени (ПЦР-РВ) с использованием набора реагентов «АмплиСенс® ВПЧ ВКР генотип-титр-FL» (Центральный НИИ эпидемиологии Роспотребнадзора – ЦНИИЭ, Россия). Экстракцию ДНК выполняли с помощью комплекта реагентов «АмплиСенс® ДНК-сорб-Д» того же производителя.
В исследование были включены ОНП из полногеномных ассоциативных исследований и исследований случай–контроль [12], значимо отличающиеся между выборками женщин с РШМ и группой сравнения: rs55986091 в гене HLA-DQB1, rs2516448 в MICA и rs9271898 в HLA-DQA1.
ОНП в локусах rs55986091, rs2516448, rs9271898 определяли по методикам, представленным ранее [13].
ПЦР-смесь объемом 25 мкл включала: праймеры, зонды и dNTP (0,44 мM) – 10 мкл; «Полимераза TaqF» – 0,5 мкл и «ОТ-ПЦР-смесь-2 FEP/FRT» – 4,5 мкл; объем выделенной ДНК – 10 мкл. ПЦР-РВ проводили на приборе Rotor GeneQ (Qiagen, Германия) по следующей программе: 95 ºС – 15 мин (1 цикл); 95 ºС – 5 с/60 ºС – 20 с/72 ºС – 10 с (45 циклов с детекцией флуоресцентного сигнала на стадии 60 ºС). При анализе результатов амплификации пороговую линию проводили на уровне 10% от максимального значения флуоресцентного сигнала для каждого канала детекции (Green, Yellow). Использовали комплекты и наборы реагентов, произведенные ЦНИИЭ (Россия).
Секвенирование продуктов ПЦР осуществляли с использованием секвенаторов PyroMark Q24 (Qiagen, Германия) и 3500xL (Applied Biosystems, США), а также реагентов и дополнительного оборудования, рекомендованных производителями.
Статистические расчеты выполнены в среде R: логистическая регрессия – с помощью пакета «tidymodels», случайные леса, GBM и XGBoost – с помощью пакетов «randomForest», «gbm», «xgboost» соответственно, обучение нейронных сетей – с помощью «neuralnet».
Кросс-валидацию осуществляли с использованием деления использованной выборки на тренировочное и тестируемое множество. Обучение моделей проводили на тренировочном множестве, которое выделено из выборок с помощью методов Фишера и Йейтса и составляло 66%. Тестирование моделей и расчет показателя точности выполнены на оставшемся множестве, p-значение < 0,05 подвергнуто поправке на множественную проверку гипотез методом Холма–Бонферрони.
Все модели сравнивали с помощью метода, описанного C.S. Moskowitz и соавт. [14].
Результаты
Пробы ДНК стратифицированы на 2 группы в зависимости от характера интраэпителиальных поражений: NILM – женщины с положительными результатами ВПЧ-теста и отсутствием интраэпителиальных поражений и РШМ – женщины с положительными результатами выявления ВПЧ и гистологически подтвержденным РШМ.
Подробная информация о группах и частоте встречаемости генотипов представлены в табл. 1 и 2 соответственно.
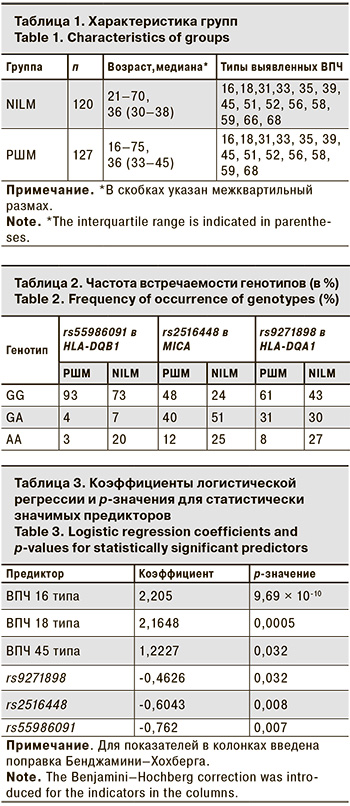
Предикторы, показывающие статистически значимую ассоциацию с риском развития РШМ, выбраны с помощью метода лассо-регрессии и расчета p-значения методом Вальда. Среди переменных наличие одного или нескольких типов и наличие одного из 3 генотипов в rs55986091, rs2516448, rs9271898 показало устойчивую ассоциацию с РШМ наличие ВПЧ 16, 18, 45 типа и 3 полиморфных варианта, получившиеся коэффициенты и p-значения представлены в табл. 3.
Логистическая регрессия, выполнив 200 шагов обучения на тренировочном множестве, нашла оптимальным значение штрафа для переменных предикторов, равное 1-10. После проверки на тестовом множестве модель показала точность, равную 0,72, положительную прогностическую ценность (ППЦ), равную 0,71, и отрицательную прогностическую ценность (ОПЦ), равную 0,75.
Далее для расчета использован метод случайных лесов, который строит множество деревьев классификации и прогнозирует ответ на основании решения большинства деревьев. Для расчета количества деревьев использованы критерии общей доли ошибок, ошибок положительного исхода (наличия РШМ) и ошибок отрицательного исхода (отсутствие РШМ). Расчет на обучающем множестве показал, что использование больше чем 200 деревьев не снижает количество ошибок и переобучает модель. Экстраполяция модели на тестируемое множество с использованием более 200 деревьев увеличивает число ошибок. Таким образом, для расчета на тестовом множестве использовалась модель, содержащая 200 деревьев.
Проверка модели на тестовом множестве показала, что точность равна 0,75, ППЦ – 0,7, ОПЦ – 0,78.
Метод GBM прогнозирует данные на основе взвешенной функции потерь от каждого следующего дерева. Модель GBM содержала вариативные показатели: число деревьев, максимальное число узлов в каждом дереве, сжатие (штраф, накладываемый на каждое следующее дерево), минимальное число наблюдений в конечном узле. Протестировано 288 моделей с различными вариантами показателей на обучающем множестве и выбрана модель с наименьшим числом ошибок: число деревьев – 2689, максимальное число узлов – 5, сжатие – 0,3, минимальное число наблюдений в конечном узле – 5. Расчет модели на тестовом множестве показал, что точность равна 0,73, ППЦ – 0,71, ОПЦ – 0,75.
XGBoost – алгоритм градиентных деревьев, схожий с методом GBM, но использующий более усовершенствованный алгоритм градиентного спуска при добавлении новых деревьев. Расчет числа деревьев на обучающем множестве выполняли с оценкой функции отрицательного логарифмического правдоподобия. При использовании 100 деревьев эта оценка составляла 0,24 на обучающем множестве. Использование более 100 деревьев увеличивало число ошибок на тестируемом множестве.
Проверка модели на тестовом множестве показала, что точность равна 0,88, ППЦ и ОПЦ – 0,88.
Сеть искусственных нейронов класса многослойного персептрона – математическая модель c прямой связью, в которой каждый нейрон получает данные от предыдущего слоя. Путем тестирования из множества вариантов выбрана модель, состоящая из входного слоя, двух скрытых внутренних слоев по 6 и 3 нейрона соответственно и выходного слоя. Модель обучена путем перебора значений весов и порогового значения для ответа. Протестировав 500 000 различных вариантов, выбрана нейронная сесть с долей ошибок на обучающем множестве 0,01 и пороговым значением 0,52.
Проверка модели на тестовом множестве показала, что точность равна 0,95, ППЦ – 0,90, ОПЦ – 0,98.
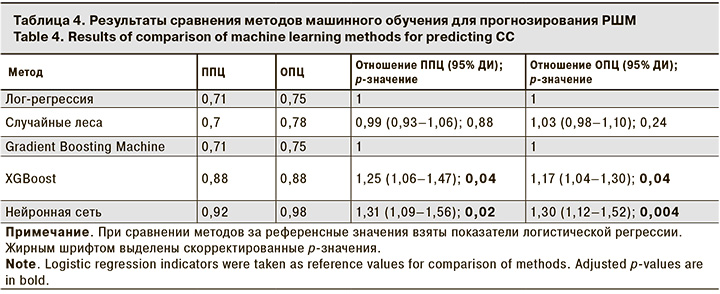
При сравнении методик прогнозирования не установлено статистически значимых различий между методами логистической регрессии, случайными лесами и GBM. Получившиеся значения для логистической регрессии являлись референсными, с которыми сравнивали остальные методики. Статистически значимые различия при сравнении со значениями логистической регрессии установлены для метода XGBoost и нейронной сети. При сравнении метода XGBoost и нейронной сети получены статистически значимые различия только для предсказания отсутствия РШМ (p-значение = 0,02), при этом после поправки на множественное тестирование показатель p-значения перестал указывать на статистически достоверные различия (p > 0,05). Такой результат интерпретирован как наличие различий на уровне статистической тенденции (табл. 4).
Обсуждение
Исследование и оценка связи полиморфных последовательностей в ДНК с мультифакторными заболеваниями на сегодняшний день является одной из самых сложных задач. Это связано с тем, что большинство заболеваний обусловлено многообразием сочетаний неблагоприятных генетических факторов с определенными условиями окружающей среды [5]. Поиск и анализ данных детерминант в сочетании с условиями окружающей среды для прогноза и стратификации популяции по степени риска – одна из ключевых целей эпидемиологических исследований [15]. Многообразие генетических и средовых факторов позволяет выделить группы риска и с помощью методов статистического анализа прогнозировать исход заболеваний.
Использование машинного обучения – один из эффективных способов увеличить точность прогнозирования и уменьшить время на расчет математических моделей [10].
В данном исследовании использованы 5 методов машинного обучения для прогнозирования РШМ у ВПЧ-инфицированных: логистическая регрессия, случайные леса, GBM, XGBoost и нейронная сеть класса многослойного персептрона.
Результаты точности прогнозирования для логистической регрессии ниже по сравнению с более сложными методами, так как логистическая регрессия при относительно простом алгоритме решения плохо справляется со сложными задачами и обладает низкой точностью, когда предикторы не имеют высокого значения коэффициента, как, например, генетические факторы с низким фенотипическим проявлением в популяции [16].
При этом методы случайных лесов и GBM не показали лучшего результата, хотя обладают двумя различными алгоритмами прогнозирования путем классификации [10]. Возможное предположение о более низкой точности классификации этих методов по сравнению с XGBoost заключается в том, что XGBoost для обучения не требует больших размеров выборки для точного прогноза.
Нейронная сеть класса многослойного персептрона показала наиболее высокие значения ППЦ и ОПЦ, при этом статистически значимо не отличаясь при предсказании наличия РШМ. Нейронные сети в своей структуре копируют модель нейронов головного мозга: входной, внутренний и выходной слои [11]. Такая структура, наряду с рандомизацией весов для каждого нейрона, позволяет делать очень точные прогнозы и обрабатывать большие объемы данных за относительно короткое время. Ранее уже было показано, что нейронные сети обладают большим потенциалом для генетической эпидемиологии [11], задача которой заключается в оценке влияния генетических факторов в сочетании с условиями окружающей среды, включающими также образ жизни, на развитие заболеваний в популяциях [17].
Представленное исследование включало некоторые допущения, которые могли повлиять на конечный результат: не учитывалась концентрация каждого типа ВПЧ, результаты не реплицированы на других выборках. В последующих работах часть этих допущений планируется учесть, а также использовать более сложные методы прогнозирования, такие как глубокое обучение, то есть обучение без учителя.
Ввиду длительного периода развития (8–10 лет) любой случай инвазивного РШМ может считаться последствием упущенных возможностей диагностики предраковых состояний. Скрининг на РШМ с весьма высокой чувствительностью выявляет цервикальные интраэпителиальные неоплазии и карциномы [7]. А.Д. Каприн и соавт. [7] обозначили 2 подхода к скринингу: организованный, при котором выявляют группы женщин и приглашают к обследованию, и спорадический – обследование женщин, обратившихся в лечебное учреждение. При этом первый вариант более эффективен. Согласно клиническим рекомендациям «Цервикальная интраэпителиальная неоплазия, эрозия и эктропион шейки матки» [18, 19], представляется важным добавить ВПЧ-тестирование для женщин старше 30 лет. Американское общество кольпоскопии и патологии шейки матки ввело рекомендации к скринингу и лечению пациенток, раз речь идет о РШМ, основанные на оценке индивидуального риска, используя математические формулы, а конкретно – смешанную модель распространенности–выживаемости [20]. Массовый скрининг с оценкой и анализом факторов риска РШМ и использованием математических моделей сможет внести весомый вклад в элиминацию данной патологии.
Заключение
Впервые проведено тестирование 5 методов машинного обучения для прогнозирования РШМ у ВПЧ-инфицированных: логистическая регрессия, случайные леса, GBM, XGBoost и нейронная сеть класса многослойного персептрона.
Использование нейронных сетей и XGBoost для прогнозирования исхода заболевания с использованием данных о генетической предрасположенности показало более точные результаты по сравнению с другими методами и может быть рекомендовано для практического применения. Модели расчета, основанные на машинном обучении, и факторы генетической предрасположенности могут быть использованы для расчета индивидуального риска РШМ, определения групп риска и коррекции периода между скринингами.



