В настоящее время все большее внимание исследователей обращается на формирование не только гуморального, но и клеточного иммунитета при инфекционных заболеваниях. По данным иностранной литературы, при коклюше специфический Т-клеточный иммунитет имеет большое значение. Так, антиген-специфические Т-клетки могут играть ведущую роль в эрадикации возбудителя и обеспечивают более длительное сохранение постинфекционного и поствакцинального иммунитета [1, 2].
Проводятся исследования по сравнению способности различных вакцин против коклюша вызывать формирование Т-клеточного иммунитета [3–9]. В то же время постинфекционный Т-клеточный иммунитет против коклюша исследован в основном ретроспективно [10, 11], его формирование в процессе заболевания практически не изучено.
При проникновении B. pertussis в организме запускается иммунный ответ, регулируемый Т-хелперами 1-го типа и Т-хелперами, продуцирующими интерлейкин-17 (ИЛ-17) (Th1/Th17-регулируемый ответ), в ходе которого формируются Т-клетки памяти [1, 2]. С другой стороны, формирование антител против B. pertussis и увеличение их авидности регулируется Т-хелперами 2-го типа (Th2). Активность Th1 и активность Th2 в какой-то мере конкурируют друг с другом, что можно проследить по изменениям в цитокиновой сети [1, 2, 12–14]. Ранее нами было проведено исследование цитокиновой регуляции гуморального иммунного ответа у больных коклюшем, как непривитых, так и привитых против этой инфекции, что позволило выявить различия в зависимости от вакцинного анамнеза [14].
Цель работы – изучение взаимосвязи формирования специфического Т-клеточного и гуморального иммунитета и его цитокиновой регуляции в динамике заболевания коклюшем у детей.
Материалы и методы
Обследование 100 детей, больных коклюшем, находившихся в 2015–2019 гг. на лечении в ИКБ № 1 г. Москвы, было 2-кратным: при госпитализации (на 2–5-й неделе заболевания) и в периоде реконвалесценции (до 12 нед. с момента постановки диагноза). Среди обследованных пациентов было 62 непривитых ребенка в возрасте от 2 мес. до 6 лет и 39 привитых детей 3–14 лет.
Концентрацию антител классов иммуноглобулинов (IgМ, IgG, IgА) в сыворотке крови оценивали методом иммуноферментного анализа (ИФА) в тест-системах Ridascreen/Bordetella pertussis (R-biopharm, Германия). Специфический Т-клеточный ответ оценивали по пролиферации Т-клеток после их 5-суточной инкубации на планшетах, покрытых антигенами B. pertussis из ИФА-наборов Ridascreen/Bordetella pertussis (R-biopharm), и антигенстимулированной продукции интерферона гамма (ИФН-γ), сопровождающей этот процесс [15, 16].
Баланс между активностью регуляторных клеток Th1 и Th2 определяли по соотношению митогенстимулированной продукции ИФН-γ и ИЛ-4 клетками крови пациентов [17].
Концентрацию цитокинов, продукция которых была стимулирована митогенами в образцах цельной крови пациентов или антигенами B. pertussis в образцах лимфоцитов, выделенных из крови пациентов, определяли методом ИФА с использованием тест-систем ЗАО «Вектор-Бест» (Россия).
Данные представлены как среднее (М) ± ошибка средней (m). Статистический анализ данных проведен с использованием пакета статистических программ Microsoft Excel и STATISTICA 10 (StatSoft Inc., США). Достоверность различий оценивали с помощью непараметрического U-критерия Манна–Уитни и t-критерия Стьюдента. Справедливость проверяемой гипотезы исследования оценивали по величине р-value, критическим значением которой считали p < 0,05.
Результаты
Исследование способности Т-клеток крови больного продуцировать ИФН-γ или интерлейкин-4 (ИЛ-4) дает возможность оценить активность в его иммунной системе Th1 и Th2 соответственно. При коклюше активность данных субпопуляций Т-клеток меняется в динамике заболевания и связана с регуляцией формирования гуморального иммунитета. Ранее этот процесс был изучен нами подробно [14]. В настоящей работе мы провели этот анализ для прямой оценки влияния баланса между Th1 и Th2 на формирование антигенспецифических Т-клеток в динамике заболевания коклюшем.
Уровень антител и Т-клеток памяти против B. pertussis, а также параметры цитокиновой сети оценивали в крови больных детей при поступлении в стационар (на 2–6-й неделе заболевания) и через 1–1,5 мес. в периоде реконвалесценции. Такая схема обследования позволяла охватить период до 12 нед. от начала заболевания, причем численность групп на большинстве сроков достигала 16–25 детей, а после 10-й недели – 10–12. Следует отметить, что после 5-й недели заболевания нарастает массив данных, полученных при повторном обследовании пациентов. Если на 5-й неделе их доля составляет около 50% в группе, то на 6–7-й неделе их уже 82%, а после 8-й недели – 100%.
У непривитых больных коклюшем анализ соотношения между активностью Th1 и Th2 по продукции характерных для них цитокинов подтвердил полученные ранее данные о постепенном переходе от активного функционирования Th1 на 1–3-й неделях заболевания к возрастанию активности Th2, регулирующих образование антител против B. pertussis (табл. 1).
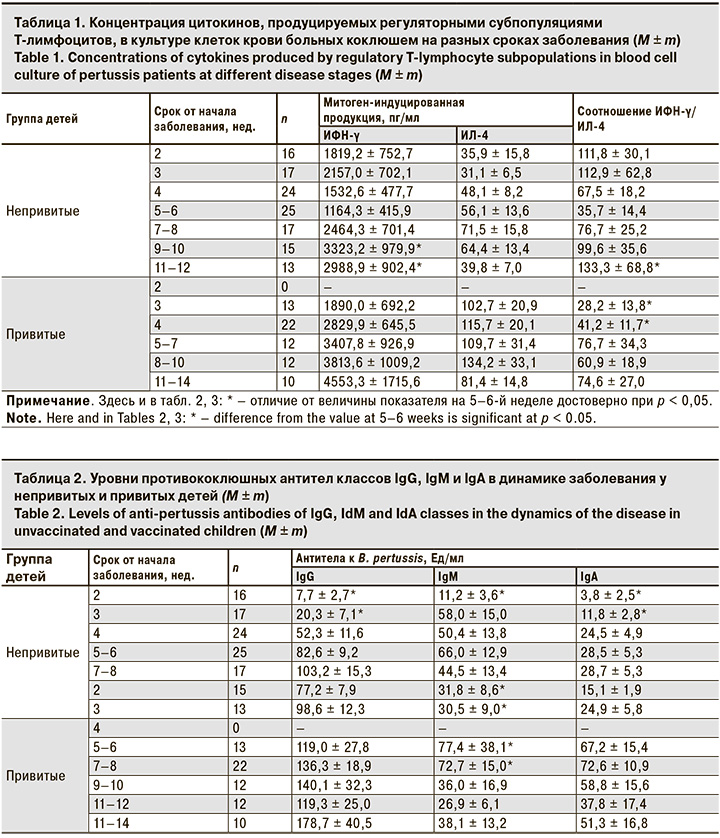
Поскольку на 5-й неделе показатели баланса между Th1 и Th2, а также регулируемые ими показатели гуморального и клеточного иммунного ответа претерпевают наиболее важные изменения, в таблицах статистическая оценка результатов проведена именно по отношению к 5-й неделе.
Наблюдается увеличение продукции ИЛ-4 Т-лимфоцитами крови и уменьшение продукции ими ИФН-γ. Величина соотношения ИФН-γ/ИЛ-4 на 4–5-й неделях заболевания у больных коклюшем, непривитых против этой инфекции, снижается в среднем в 2–3 раза, а затем восстанавливается. У ранее привитых больных коклюшем, напротив, самые низкие показатели ИФН-γ/ИЛ-4 характерны для 3–4 нед. заболевания, а затем этот показатель увеличивается в 1,5–2 раза.
На формировании антител изменения в цитокиновой сети сказываются следующим образом (табл. 2).
У непривитых пациентов на начальных этапах заболевания преобладает Th1/Th17-регуляция иммунного ответа. Антитела в сыворотке крови представлены в основном IgM. Затем под влиянием нарастающей активности Th2 происходит переключение изотипа антител, и на 5-й неделе в сыворотке крови устойчиво преобладают IgG. IgА на этом сроке регистрируются более чем у 2/3 больных. На 5-й неделе активность Th1 минимальна, а далее наблюдается совместное повышение активности Th1 и Th2 (уровней продукции ИФН-γ и ИЛ-4), что приводит к повышению соотношения ИФН-γ/ИЛ-4. Вероятно, такая активность Т-клеток связана с тем, что выраженный клеточный ответ сочетается в это время с развивающейся продукцией антител.
У ранее привитых детей при заболевании коклюшем с самых ранних сроков в сыворотке крови определяются не только IgМ, но и IgG, IgА. У них реализуется вторичный иммунный ответ на антигены B. pertussis, который также обеспечивается смещением баланса в сторону преобладания Th2 и низкими значениями соотношения ИФН-γ/ИЛ-4 до 5-й недели заболевания. После 5-й недели от начала заболевания средняя концентрация IgM в сыворотке крови больных падает, соотношение ИФН-γ/ИЛ-4 повышается за счет увеличения продукции ИФН-γ при стабильно высоких показателях ИЛ-4. Таким образом, мы наблюдаем не только бустирование гуморального ответа, но и реактивацию клеточного ответа на инфекцию.
Для изучения формирования Т-клеток памяти из крови детей, больных коклюшем, были выделены лимфоциты и проведена их антигенная стимуляция in vitro. В течение 5 сут. лимфоциты, способные распознавать антигены B. pertussis, пролиферировали, а происходящая при этом продукция ими ИФН-γ однозначно показывала, что антигенраспознающие клетки являются Т-лимфоцитами [1, 16]. Для каждого срока заболевания вычислено среднее увеличение концентрации ИФН-γ в присутствии антигена. Также сделана индивидуальная оценка, имеются ли в крови больного Т-клетки памяти, и в каждой группе определен процент больных с положительными пробами, содержащими не менее 50 пг/мл ИФН-γ.
Данные, представленные в табл. 3, свидетельствуют о том, что у 69–72% непривитых детей антигенспецифические (АГ-специфические) Т-клетки выявляются на 2–3-й неделе заболевания (пока в их крови нет антител или есть только IgM в высоком титре). Затем процент проб с Т-клетками, распознающими антигены B. pertussis, резко падает до 54,2% на 4-й и до 36,0% на 5-й неделе. Начиная с 7-й недели, в крови больных вновь выявляют и стабильно регистрируют до 12 нед. АГ-специфические Т-клетки, причем у 75–92% пациентов.
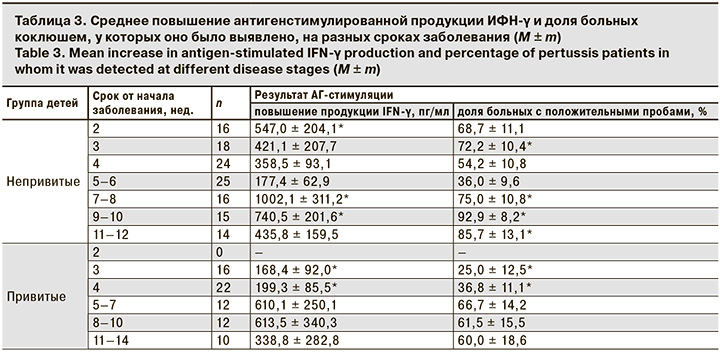
Напротив, у привитых детей в начале заболевания АГ-специфические Т-клетки выявляются менее чем в половине проб. На 5–7-й неделе доля больных, в крови которых обнаруживаются Т-клетки памяти, повышается, но все равно остается ниже, чем в группе непривитых.
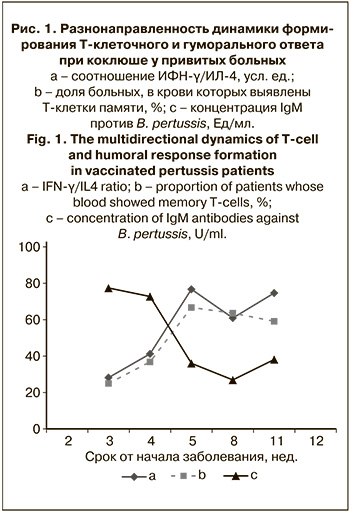
Взаимосвязь между приведенными в табл 1–3 показателями специфического Т-клеточного и гуморального иммунитета, а также цитокиновой регуляцией их формирования в динамике заболевания графически представлена на рисунках.
На рис. 1 видно, что у привитых детей, переносящих коклюш, на 5-й неделе заболевания увеличивается доля больных с АГ-специфическими Т-клетками в крови и одновременно устойчиво снижается сывороточная концентрации IgM.
У непривитых детей (рис. 2) от 2-й до 5-й недели заболевания происходят нарастание сывороточной концентрации IgM и снижение доли больных с АГ-специфическими Т-клетками в крови. Затем баланс Th1 и Th2 резко меняется, IgM постепенно исчезают из крови, а Т-клетки памяти выявляются у все большего числа больных.
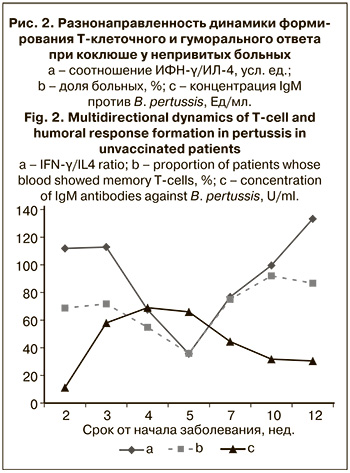
В обоих случаях динамика формирования Т-клеточного иммунитета приближена к динамике баланса Th1 и Th2, а динамика продукции антител IgM против B. pertussis противоположна ей.
Обсуждение
Полученные данные показывают, что при заболевании у детей, привитых против коклюша, независимо от сроков после проведенной вакцинации, бустирует специфический гуморальный ответ, который поддерживается повышенной активностью Th2. Интенсивность продукции ИЛ-4 у привитых детей на всех сроках превышает таковую у непривитых, но в обоих случаях изменение баланса между Th1 и Th2 в большей степени зависит от изменения продукции ИФН-γ, чем от продукции ИЛ-4. Поэтому с повышением активности Th1, продуцирующих ИФН-γ, после 5-й недели от начала заболевания активизируется формирование Т-клеточного иммунитета.
Среди привитых доля детей, в крови которых обнаруживаются Т-клетки памяти, вплоть до 12-й недели от начала заболевания не превышает 67%, несмотря на то, что у них иммунный ответ развивается как вторичный. Возможно, как обсуждается в иностранной литературе, это связано с широким применением бесклеточных вакцин для профилактики коклюша [1, 3, 18].
Непривитые пациенты активно развивают специфический Т-клеточный иммунитет с ранних сроков заболевания коклюшем. На 2-й неделе в крови только у 3 (17,6%) пациентов обнаруживали IgM к возбудителю коклюша, а Т-клетки, способные распознавать антигены B. pertussis и активироваться, продуцируя ИФН-γ, были выявлены в этой группе у 68,7% детей.
Снижение доли больных с АГ-специфическими Т-клетками в крови совпадает с резким повышением уровня IgG и увеличением активности Th2, с одной стороны, и подавлением активности Th1 – с другой. По-видимому, за эти 2 нед. увеличение численности Т-клеток памяти замедляется, а уже сформировавшиеся Т-клетки, место действия которых при коклюше – в основном лимфоидная ткань легких и верхних дыхательных путей, в меньшем количестве выходят в циркулирующую кровь.
Восстановление и стремительное увеличение доли положительных проб с АГ-специфическими Т-клетками совпадает с 1,5–2-кратным ростом продукции ИФН-γ и сохранением ее на уровне 2400–3400 пг/мл.
Тот факт, что после перенесенного заболевания в периоде реконвалесценции не у всех детей в крови выявляются Т-клетки памяти, по мнению отдельных авторов [19], может быть связан, в частности, с влиянием на формирование Т-клеточного иммунного ответа антибиотикотерапии.
Заключение
Результаты исследования показывают, что АГ-специфические Т-клетки могут быть обнаружены в крови непривитых детей, начиная с ранних сроков заболевания коклюшем. У большинства привитых больных такие клетки появляются в циркулирующей крови после завершения бустерного образования антител. Динамика цитокиновой регуляции антителообразования, закономерной для определенных сроков заболевания коклюшем, находит отражение в процессе формирования Т-клеток памяти.



