Туляремия (Т) продолжает оставаться актуальной проблемой, так как использование ее возбудителя потенциально возможно с террористической целью [1–5]. В отдельные годы проявления инфекции принимают характер эпидемических вспышек вследствие активизации ее природных очагов и снижения объемов профилактических мероприятий, при этом имеют место гиподиагностика заболевания и антивакцинальные настроения среди населения. Несмотря на то что на современном этапе Т приобретает урбанистический характер, влияние абиотических факторов на эпидемический и эпизоотический процессы этой инфекции изучены недостаточно [6–8]. В настоящее время в новом субъекте Российской Федерации – Донецкой Народной Республике (ДНР), охваченной военным конфликтом, отмечаются рост заболеваемости Т и формирование очагов на территориях, относимых к неэндемичным [9]. ДНР расположена в степной зоне. Исследования З.М. Нехороших и соавт. [10] показали, что в указанной зоне большинство природных очагов Т активны. В связи с этим особую значимость приобретают контроль над их эпизоотическим состоянием и прогнозирование эпидемического потенциала для предотвращения развития эпидемиологических последствий. В Ставропольском крае в степной зоне с 2003 по 2018 г. преобладали случаи заражения через инфицированную воду местных водопроводов, в том числе групповые, что диктует необходимость постоянного контроля за их сохранностью (грызунонепроницаемостью) [11]. Это подтверждает сообщение A. Hennebique и соавт. [12] о том, что в последние десятилетия во всем мире регистрировались вспышки и спорадические случаи Т, передающейся через воду, вызванные новыми водными видами Francisella, способными длительно выживать в водной среде [4], образуя биопленки [7].
С 1944 г. по май 2023 г. в Донецкой области (по 2014 г.) и ДНР (2015 г. – май 2023 г.) было зарегистрировано 283 случая Т у людей. Если с 1991 по 2000 г. среднемноголетний показатель заболеваемости составил 0,024 на 100 тыс. населения, то с 2001 по 2010 г. он вырос в 1,3 раза и составил 0,03 случая на 100 тыс. населения [9]. Отмечались спорадические заболевания – 1–3 случая с 2002 г. по 2007 г. Уровень заболеваемости колебался от 0,02 до 0,06 на 100 тыс. населения. Единичные случаи Т регистрировали из-за снижения иммунной прослойки среди населения, проживающего и работающего на энзоотичных территориях. За период 2011–2020 гг. зарегистрировано 14 случаев, а в 2008–2015 гг., то есть в течение 8 лет, случаи Т у людей отсутствовали. Однако в 2016 г. в Новоазовском районе возникла вспышка заболевания, интенсивный показатель составил 0,38 на 100 тыс. населения, что в 9,5 раза выше по сравнению с 2007 г. Показатель заболеваемости Т населения ДНР в 2016 г. был сформирован в связи с регистрацией случаев среди лиц негражданского сектора (профессионально-угрожаемые контингенты). В 2019 г. выявлено еще 5 случаев Т (0,22 на 100 тыс. населения), 3 из которых территориально связаны с предыдущей вспышкой, а 2 установлены ретроспективно в результате проведения мониторинга за иммунной структурой населения в отношении Т.
Среднемноголетний показатель заболеваемости за 2011–2020 гг. составил 0,30 на 100 тыс. населения и в 10 раз превысил показатель 2001–2010 гг. Полученные результаты свидетельствуют о выраженной тенденции к росту заболеваемости Т в ДНР в течение последних 30 лет. Темп прироста в 2001–2010 гг. по сравнению с предыдущим десятилетием составил 25%, а в 2011–2020 гг. по сравнению с предыдущим периодом – 900 %.
После 40-летнего затишья с 1987 г. на территории Донецкой области снова начали регистрировать вялотекущие эпизоотические процессы Т с их периодической активизацией. Численность животных – резервуаров инфекции в отдельные годы (1993, 2001, 2002, 2004) достигала высокого уровня. Количество энзоотичных территорий ежегодно увеличивалось и выросло с 2 населенных пунктов в 1987 г. до 79 (в 4 городах и 16 районах) в 2020 г. В 2014 г. процент пораженных Т территорий в ДНР, в том числе временно подконтрольных Украине, составил 34,5%.
Цель исследования – определение критериев эпидемического благополучия и предвестников эпидемического неблагополучия для усовершенствования системы комплексного мониторинга за туляремийной инфекцией.
Материалы и методы
Проанализированы данные 30-летнего наблюдения за природными очагами Т. Для этого использованы данные о заболеваемости Т из статистических отчетов Донецкой областной санитарно-эпидемиологической станции (1991–2014 ) и Республиканского центра санитарно-эпидемиологического надзора Государственной санитарно-эпидемиологической службы Министерства здравоохранения ДНР (2015–2022): «Отчет об отдельных инфекционных заболеваниях» формы № 1 и 2 (месячная и годовая); отраслевые отчеты о результатах эпизоотического мониторинга за Т. Для характеристики эпизоотической обстановки в очагах использовали зоолого-паразитологические, бактериологические и серологические методы исследования.
Метод ретроспективного эпидемиологического анализа был использован для установления эпидемиологических особенностей Т в Донецком регионе. С помощью клинического метода изучали наиболее часто встречающиеся формы заболевания, что позволило определить основные пути заражения в ДНР. Для создания банка данных изучено 20 «Карт эпизоотологического и эпидемиологического обследования очага зоонозного заболевания» (ф. № 391/у). При изучении состояния как активного, так и поствакцинального противотуляремийного иммунитета использованы методы оценки специфической сенсибилизации (кожная проба с тулярином) и реакций прямой агглютинации (РА) и непрямой гемагглютинации (РНГА) с целью диагностики Т и проведения серологического скрининга лиц негражданского сектора.
В работе были использованы реагенты:
- туляремийный эритроцитарный антигенный диагностикум (Ставропольский научно-исследовательский противочумный институт Роспотребнадзора, Россия);
- сыворотка туляремийная диагностическая сухая для РА (Иркутский ордена Трудового Красного Знамени научно-исследовательский противочумный институт Сибири и Дальнего Востока Роспотребнадзора, Россия).
Для мониторинга за циркуляцией возбудителя Т в объектах внешней среды за период 1993–2022 гг. было собрано и исследовано 28 997 экземпляров мышевидных грызунов, 37 604 экземпляра иксодовых клещей, 6401 погадка хищных птиц, 925 зайцев, 942 пробы воды естественных водоемов. Методом РНГА исследовали погадки хищных птиц, представляющие собой спрессованные непереваренные остатки пищи животного происхождения (кости, шерсть мышевидных грызунов, перья, хитин насекомых и т. п.), отрыгиваемые некоторыми хищными птицами в виде округлого комка. С помощью этого метода определялся титр антител к Т в останках грызунов, находившихся в погадках. Всего за годы наблюдения исследовано 1236 погадок.
При исследовании мышевидных грызунов, отловленных в очагах заражения людей в Новоазовском районе в 2016 г., бактериологически были выделены 5 культур Francisella tularensis биовар II ery R, определена чувствительность к антибиотикам. Установлена резистентность штамма к ампициллину, цефотаксиму, эритромицину, клиндамицину, полимиксину; а также чувствительность к гентамицину, фторхинолонам, рифампицину, доксициклину, левомицетину. В 2022 г. при исследовании воды в реке Грузский Еланчик (Тельмановский район) выделено 4 культуры Francisella tularensis, подвид holarctica, биовар II, erу R (эритромицинустойчивый), аналогичные культурам, полученным в 2016 г.
Для математической обработки данных применяли стандартные пакеты программного обеспечения Microsoft Office Excel (2010) в среде операционной системы Windows 7. Проектирование, построение и анализ полученных математических моделей осуществляли с применением пакетов для статистического анализа данных STATISTICA 10.0 и MedCalc 11.6.
При статистической обработке данных были использованы базовые методы математической статистики: описательная статистика (величины в виде выборочного среднего значения, стандартной ошибки средней величины (M ± m), 95% доверительного интервала), критерии парных и множественных сравнений. Значимость статистических различий средних величин выборок оценивали с помощью параметрических ( t-критерия Стьюдента и F-критерия Фишера ) и непараметрических критериев (W-критерия Уилкоксона, Chi-square test, критерия Манна–Уитни при асимметрии распределения).
Также использованы методы построения математических моделей многофакторной линейной регрессии с алгоритмами «включения–исключения» для пошаговой многомерной регрессии. Для анализа таблиц сопряженности использовали критерий χ2 Пирсона или угловое преобразование Фишера.
Результаты
Эпидемический процесс Т в Донецкой области и ДНР в течение трех десятилетий характеризовался однотипным проявлением заболеваемости. В 1991–2000 гг. Т была свойственна летне-осенняя сезонность, связанная с заражением во время отдыха на природе. С 2001 по 2020 г. сезонность изменилась на осенне-зимнюю, обусловленную выполнением определенного вида профессиональных работ. Отсутствие заболеваний весной и летом свидетельствует о том, что в природных очагах Т в ДНР не реализуется трансмиссивный путь передачи. Это дополнительно подтверждают и результаты ежегодного исследования клещей на Т.
Заболевание протекало в различных клинических формах. В Донецкой области и ДНР чаще всего возникали бубонная (28,6%) и легочная (32,1%) Т. Комбинированные формы были у 5 (17,6%) больных, генерализованная – у 2 (7,1%), ангинозная и абдоминальная – по 1 (3,6%) заболевшему.
При заражении Т превалировал контактный путь передачи (42,9%), в 32,1% случаев реализовался воздушно-пылевой путь. Действие этих двух путей одновременно было установлено у 14,3% заболевших. Один больной (3,6%) заразился алиментарным путем, в двух случаях (7,1%) способ передачи возбудителя установить не удалось, так как диагноз был поставлен ретроспективно.
Несмотря на то что, по данным некоторых авторов, в настоящее время сохраняется выраженная урбанизация инфекции – более 80% заболевших составляют городские жители [13], а также дети до 14 лет, эпидемиологически значимым в ДНР является факт регистрации заболевших преимущественно в сельской местности (78,6–86,4%), к тому же 85,7–81,0% среди заболевших – взрослое население.
К отличительным признакам эпидемического процесса в последнее время, в сравнении с предыдущими десятилетиями, следует отнести и увеличение среди заболевших удельного веса лиц негражданского сектора (мужчины).
Туляремийная инфекция в ДНР характеризуется четко выраженными гендерными различиями. Из 28 случаев заболеваний, возникших в течение 30 анализируемых лет (1991–2020), 75,0% наблюдались у мужчин. Вероятно, это обусловлено более рискованными видами профессиональной деятельности у них.
В отличие от данных научной литературы о наибольшем риске и уровне заболеваемости Т лиц в возрасте 40–70 лет и наименьшем риске для молодых людей [14], в ДНР, напротив, отмечено более частое поражение лиц молодого возраста.
Проблемными в настоящее время в ДНР являются: гиподиагностика заболевания, недостаточный охват профилактическими дератизационными работами объектов эпидемического риска, антивакцинальные настроения среди населения, проведение боевых действий на территории Республики.
Позитивные результаты исследований, выявленные при мониторинге за циркуляцией возбудителя Т в объектах внешней среды за период 1993–2022 гг. (суммарно), в частности, среди мышевидных грызунов – 0,6%, погадок – 4,2%, зайцев – 3,9%, свидетельствуют о постоянной циркуляции возбудителя Т в природных очагах.
Таким образом, проведенные эпидемиологические, эпизоотологические и серологические исследования выявили особенности эпидемического процесса Т на территории ДНР, что позволило сформировать комплексную систему диагностико-прогностических критериев эпидемического процесса Т, а также основные положения оптимизации эпиднадзора за этой инфекцией в регионе.
Для улучшения санитарно-эпидемической ситуации в отношении Т на энзоотичных территориях необходимы:
- постоянный мониторинг видового состава, численности, инфицированности среди мышевидных грызунов и клещей;
- оценка климатических факторов (температура воздуха, количество осадков), которые способствуют высокому уровню эпизоотии среди источников Т;
- корректировка профилактических мероприятий с учетом активности факторов внешней среды (среднегодовая температура, численность грызунов, удельный вес положительных находок во внешней среде и т. д.);
- молекулярно-генетические исследования выделенного туляремийного микроба от больных пациентов или грызунов для изучения его свойств и оценки возможного применения в качестве биоагента;
- плановая дератизации на объектах эпидемического риска, независимо от уровня заболеваемости Т среди населения;
- мониторинг иммунологической структуры населения, проживающего на энзоотичных территориях, в том числе напряженности поствакцинального иммунитета у вакцинированных;
- взятие кожные проб с тулярином для дифференциальной диагностики внебольничных пневмоний.
Для оптимизации действующей системы эпиднадзора за Т (мониторинг за циркуляцией возбудителя во внешней среде, включающий отлов и исследование источников инфекции, отбор проб воды и т. д.; выявление и регистрация больных; мониторинг за иммунологической структурой населения, проживающего на энзоотичных территориях, и состоянием поствакцинального иммунитета) в ДНР разработаны мероприятия по улучшению эпиднадзора за этой инфекцией. Их проведение позволит повысить качество противоэпидемической и профилактической работы.
Авторами разработаны критерии эпидемического благополучия и предвестники эпидемического неблагополучия (табл. 1).

Информационная подсистема эпиднадзора за Т обеспечивает сбор и систематизацию достоверной информации о лабораторной диагностике, заболеваемости, состоянии иммунопрофилактики, влиянии социально-экологических условий. В информационной подсистеме необходимо оптимизировать проведение мероприятий на всех уровнях эпидемического процесса.
На уровне 1 «Молекулярно-генетический мониторинг за циркуляцией штаммов/изолятов возбудителя» исследования еще не внедрены в практику, тогда как именно генотипирование изолятов туляремийного микроба позволяет дифференцировать штамм возбудителя, что в современных условиях вооруженного конфликта и биоугроз становится весьма актуальным.
На уровне 2 «Мониторинг за клиническими формами заболевания» целесообразно проводить своевременное выявление и полную регистрацию всех клинических форм заболевания [15] с учетом прививочного статуса. Этот уровень предполагает контроль заболеваемости, смертности, летальности (по времени, территории, возрасту, социально-профессиональным признакам).
На уровне 3 «Мониторинг влияния биотических и абиотических факторов» важной является организация контроля за воздействием биотических и абиотических факторов внешней среды (источниками и переносчиками), который включает учет численности, видового состава грызунов и клещей, установление инфицирования (серотипирование) грызунов, клещей, других животных [6, 7, 16–18]; учет метеофакторов (температура воздуха, количество осадков, рН грунта), исследование проб воды поверхностных источников на Т [8, 19].
Уровень 4 «Оценка социальных факторов» предусматривает мониторинг иммунологической структуры населения, в том числе в рамках ретроспективного анализа. По мере снижения заболеваемости на энзоотичных территориях необходимо проводить исследование сывороток крови для изучения состояния иммунитета населения, проживающего и работающего на энзоотичных территориях. Для этого нужно подбирать лиц, у которых в анамнезе были жалобы и клинические проявления, не исключающие Т. Серологическим и аллергическим методами также следует оценивать и поствакцинальный иммунитет для своевременного проведения ревакцинации против Т1.
Этот уровень должен включать оценку состояния иммунопрофилактики (планирование и выполнение плана профилактических прививок на энзоотичных территориях, удельный вес медицинских отводов и отказов от вакцинации, анализ привитости, учет поствакцинальных осложнений и поствакцинальных реакций) [20, 21].
Основными показателями улучшения эпидемической ситуации по туляремии должны быть следующие: тенденция к снижению заболеваемости и доведению ее до спорадического уровня; удлинение межэпидемического периода заболеваемости; отсутствие сезонности и очаговости; охват вакцинацией всего населения, проживающего на энзоотических территориях.
Ретроспективный эпидемиологический анализ должен включать: определение контингентов риска, территории и времени риска; оценку эффективности проведенных профилактических и противоэпидемических мероприятий, санитарно-эпидемического состояния территорий.
Авторами установлены математические закономерности развития эпидемического и эпизоотического процессов с целью усовершенствования комплексного мониторинга системы санитарно-эпидемиологического надзора и прогнозирования заболеваемости Т.
Прогнозирование уровня заболеваемости Т осуществляли путем построения математической многофакторной модели с учетом влияния ряда независимых предикторов. В качестве входных предикторов модели были выбраны следующие факторы: годовая сумма осадков (мм); средняя годовая температура (оС); атмосферное давление (мм рт. ст.); относительная влажность воздуха (%); средняя численность мышевидных грызунов (%); удельный вес вакцинированных против Т (%); удельный вес ревакцинированных против Т (%); удельный вес площадей, обработанных дератизацией (%); удельный вес освобожденной после дератизации площади (%); удельный вес положительных находок по туляремии (серопозитивные по туляремии грызуны, погадки, присутствие возбудителя Т в речной воде и в грызунах) (%); абсолютное количество новых очагов. Предикторы принимали определенные порядковые или имели дискретные числовые значения. В качестве зависимой переменной (показателя прогноза или отклика) использовали количество заболевших Т (КЗТ) (табл. 2).
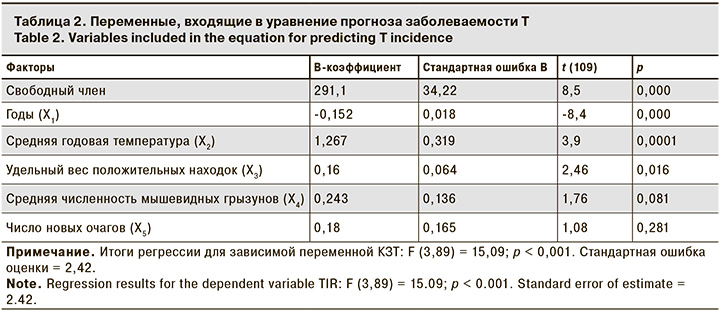
После расчета линейной модели были получено уравнение:
КЗТ = 291,1–0,152×Х1+1,267×Х2+0,16×Х3+0,243×X4+0,18×X5+0,39,
где 291,1 – свободный член регрессии и 0,39 – поправочный коэффициент.
Анализ качества модели указывает на ее достаточно высокие прогностические способности на 5 признаках.
На рис. 1 показана ROC-кривая (Receiver Operating Characteristic curve) многофакторной линейной модели прогнозирования показателя КЗТ, рассчитанной на 5 факторных признаках.
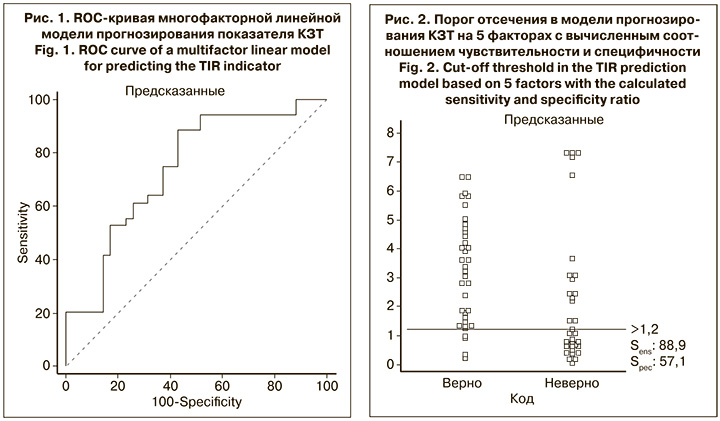
Своеобразным методом оценки ROC-кривых является оценка площади под кривыми (AUC, Area under the curve). Приблизительная шкала значений AUC, отражающая качество диагностического теста или модели, такова:
- AUC = 0,9–1,0 – отличное качество;
- AUC = 0,8–0,9 – высокое качество;
- AUC = 0,7–0,8 – хорошее качество;
- AUC = 0,6–0,7 – среднее качество;
- AUC = 0,5–0,6 – плохое (неудовлетворительное) качество.
Расчетное значение AUC в модели прогнозирования показателя КЗТ равно 0,713 ± 0,061 (95% ДИ 0,594–0,815), что соответствует значению «хорошее качество». Расчетное значение чувствительности (Sens.) модели составило 88,9 (95% ДИ 73,9–96,8), а специфичности (Spec.) – 57,1 (95% ДИ 39,4–73,7) при наличии значения порога отсечения на уровне > 1,2053 (рис. 2).
По знаку В-коэффициента модели и величине отношения шансов (ОШ) можно судить о степени влияния каждого фактора на уровень заболеваемости Т (табл. 3).
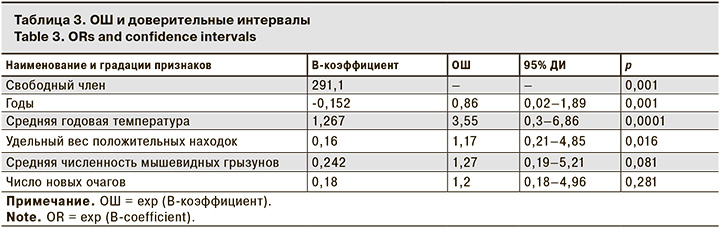
Проведенный многофакторный анализ показал, что относительный риск заражения людей Т увеличивают:
- повышение среднегодовой температуры на 1 °С – в 3,6 раза (р < 0,05);
- увеличение средней численности мышевидных грызунов на 1 особь – в 1,27 раза (р > 0,05);
- рост удельного веса положительных находок среди мышевидных грызунов на 1 зараженную особь – в 1,17 раза (р < 0,05);
- число новых очагов на 1 единицу – в 1,2 раза (р > 0,05).
Управленческая подсистема эпиднадзора за Т оценивает качество противоэпидемической, профилактической, организационной, методической, управленческой работы в оперативном и ретроспективном плане для прогнозирования тенденции в развитии эпидемического процесса Т. На этой основе управленческая подсистема формулирует тактические и стратегические решения в борьбе с Т [22].
Принятие управленческого решения включает планирование мероприятий на следующий год, на перспективу; проведение ежегодной корректировки планов; экстренное проведение противоэпидемических мероприятий. Система реализации мероприятий включает оздоровление очагов с проведением гидромелиоративных работ; борьбу с мышевидными грызунами как в хозяйственных постройках, помещениях, так и в открытых полевых стациях; проведение комплекса санитарно-гигиенических мероприятий2.
Мероприятия в открытых полевых станциях включают соблюдение сроков и качества распашки полей; сбор урожая с минимальными потерями; уничтожение разрастания бурьянов; комплекс дератизационных и дезинсекционных мероприятий [23].
Для успешной реализации мероприятий, предусмотренных планами по предупреждению эпидемических осложнений по Т, необходимы контроль выполнения управленческих решений, в том числе за полнотой, своевременностью, качеством исполнения, а также обратная связь с исполнителями мероприятий2.
Обсуждение
Вооруженный конфликт и прекращение вакцинации в ДНР привели к повышению активности эпидемического процесса в природных очагах среди животных и значительному росту заболеваемости Т людей, поскольку с 2016 г. по май 2023 г. было зарегистрировано 72 местных случая заболевания, что составило 25% всех случаев Т в регионе за 79 лет наблюдения.
Проведенные эпидемиологические, эпизоотологические и серологические исследования выявили особенности эпидемического процесса Т на территории ДНР, что позволило сформировать комплексную систему диагностико-прогностических критериев эпидемического процесса Т, а также основные положения оптимизации эпиднадзора за этой инфекцией в регионе.
Полевыми исследованиями, проведенными специалистами Одесского противочумного института, установлено, что на юге Украины в степной зоне также существуют благоприятные экологические условия для персистенции F. tularensis, увеличения численности диких млекопитающих и их миграции, что служит фактором распространения инфекции и расширения территорий и активизации природных очагов Т [10].
Повышение эпидемической активности природных очагов Т связано с ослаблением организации и проведения профилактических и противоэпидемических мероприятий. В то же время Т относится к управляемым инфекциям, при которых специфическая профилактика является одним из главных звеньев в системе эпиднадзора. Поэтому сейчас в ДНР необходима организация активной профилактической иммунизации (вакцинации и ревакцинации) контингентов населения, принадлежащих группам потенциального риска заражения на энзоотических территориях. Известно, что эпидемиологическое благополучие населения определяется уровнем иммунной прослойки, которая должна составлять не менее 80–90%. Контроль за состоянием иммунитета населения должен осуществляться посредством туляриновой пробы, однако тулярина в ДНР нет.
Комплексное использование предложенных информационной, диагностико-прогностической и управленческой систем позволит своевременно предвидеть эпидемическое и эпизоотическое неблагополучие и разработать научно-обоснованные рекомендации по проведению целевых профилактических и противоэпидемических мероприятий среди групп риска. В итоге это будет способствовать снижению заболеваемости до спорадических случаев и предупреждению тяжелых форм инфекции [24, 25].
Недостатки эпиднадзора за Т на социально-экосистемном уровне связаны с проблемами управленческой подсистемы эпиднадзора, которая из-за отсутствия материальных ресурсов и обоснованности их целесообразности не может удовлетворить потребность в планировании и выполнении рациональных мер борьбы с Т. Таким образом, существующая система эпидемиологического надзора недостаточно эффективна и требует усовершенствования на всех уровнях его проведения.
Заключение
Для оптимизации действующей системы эпиднадзора за Т авторами разработана комплексная структурно-функциональная схема надзора за этой инфекцией. Предложены новые подходы к структуре информационной подсистемы и функционирования ее составляющих, конкретные мероприятия для мониторинга Т, базирующиеся на специфике инфекции и принципах системного подхода к эпидемическому процессу. Использование модели позволит повысить качество противоэпидемической и профилактической работы. Усовершенствование эпидемиологического надзора за Т заключается в эффективном использовании имеющихся сил и средств. Поэтому объем и направленность мероприятий в отношении мониторинга природных очагов должны строиться на основании степени эпидемиологического риска инфицирования человека, что дает возможность ранжировать энзоотичные по Т территории по уровню эпидемической безопасности, прогнозировать эпидемическую ситуацию, оценивать ее с социально-экономической точки зрения и принимать управленческие решения, направленные на обеспечение эпидемического благополучия населения.



