Стрептококковые (группы А) инфекции входят в число наиболее острых проблем здравоохранения во всех странах мира. По данным ВОЗ, в мире ежегодно возникает свыше 111 млн случаев стрептодермии и 616 млн случаев стрептококковых фарингитов. В России ежегодно более 10 млн детей и лиц юношеского возраста переносят респираторную стрептококковую инфекцию.
Острые болезни органов дыхания (БОД) в настоящее время являются одной из самых актуальных проблем военной медицины в связи с высоким уровнем заболеваемости военнослужащих, проходящих военную службу по призыву [1, 2].
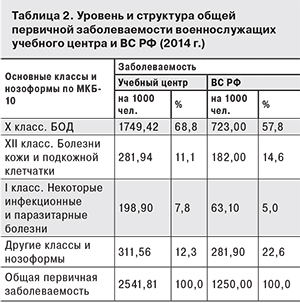
Так, по данным Главного военно-медицинского управления, в 2014 г. в структуре общей заболеваемости доля болезней органов дыхания составила более 57%.
В Вооруженных Силах (ВС РФ) стрептококковые заболевания занимают одно из первых мест среди инфекционных заболеваний военнослужащих. В качестве средства экстренной профилактики используется антибиотик бициллин‑5 [3].
 СГА имеют широкий спектр суперантигенов (САГ): эритрогенные токсины А, В и С, D, экзотоксин F (митогенный фактор), стрептококковый суперантиген (SSA), эритрогенные токсины SpeX, SpeG, SpeH, SpeJ, SpeZ, Sme Z-2. Все эти суперантигены могут взаимодействовать с антигенами главного комплекса гистосовместимости (ГКГС) II класса, экспрессированными на поверхности антиген-презентирующих клеток (АПК) и вариабельными участками бета-цепи (Vбета-рецепторами) Т-лимфоцитов, вызывая их пролиферацию и тем самым мощный выброс цитокинов, особенно таких, как фактор некроза опухоли и гамма-интерферон. Эта гиперпродукция оказывает системное воздействие на организм и приводит к разрушительным последствиям.
СГА имеют широкий спектр суперантигенов (САГ): эритрогенные токсины А, В и С, D, экзотоксин F (митогенный фактор), стрептококковый суперантиген (SSA), эритрогенные токсины SpeX, SpeG, SpeH, SpeJ, SpeZ, Sme Z-2. Все эти суперантигены могут взаимодействовать с антигенами главного комплекса гистосовместимости (ГКГС) II класса, экспрессированными на поверхности антиген-презентирующих клеток (АПК) и вариабельными участками бета-цепи (Vбета-рецепторами) Т-лимфоцитов, вызывая их пролиферацию и тем самым мощный выброс цитокинов, особенно таких, как фактор некроза опухоли и гамма-интерферон. Эта гиперпродукция оказывает системное воздействие на организм и приводит к разрушительным последствиям.
СГА способны продуцировать целый ряд других биологически активных экстрацеллюлярных веществ, таких как стрептолизин O и S, стрептокиназа, гиалуронидаза, ДНКаза В, стрептодорназа, липопротеиназа, С5а-пептидаза и др. Клеточная стенка включает капсулу, белковый, полисахаридный (группоспецифический антиген) и мукопротеидный слой. Капсула состоит из гиалуроновой кислоты и является одним из факторов вирулентности. Наряду с М-белком она обеспечивает антифагоцитарную устойчивость возбудителя. В адгезии (колонизации) поверхности клеток слизистых оболочек человека также активную роль играют М-белок, липотейхоевая кислота, F-белок.
В антигенном отношении (по М-белку) выделяют свыше 110 серотипов СГА. Известно, что ревматизм чаще всего возникает после инфицирования стрептококком М-типов 1, 3, 5, 6, 18, а гломерулонефрит – 2, 17, 19, 24, 49, 55, 57, 59 типов. В то же время известно, что стрептококки первого серотипа способны вызывать как ревматизм, так и гломерулонефрит. С экологических позиций различают «кожные» (находящиеся на кожных покровах) и «респираторные» (находящиеся в носоглотке) штаммы стрептококков [4–6].
Резервуар и источники инфекции – больные различными клиническими формами острых стрептококковых заболеваний и носители патогенных стрептококков. Наибольшее эпидемиологическое значение имеют больные с локализацией микробного очага в области верхних дыхательных путей (скарлатина, ангина). Такие больные обладают высокой заразительностью, а выделяемые ими стрептококки содержат основные факторы вирулентности: капсулу и М-белок. Поэтому заражение восприимчивых лиц от указанных больных наиболее часто заканчивается развитием у них манифестной инфекции. Лица, у которых очаги стрептококка располагаются вне дыхательных путей (стрептококковые пиодермиты, отиты, мастоидиты, остеомиелиты и т. д.), имеют меньшее эпидемиологическое значение в связи с менее активным выведением возбудителя из организма больного.
Механизм передачи инфекции в основном аэрозольный, путь передачи – воздушно-капельный. Заражение происходит, как правило, при тесном длительном общении с больным или носителем.
 Возбудитель чаще всего выделяется во внешнюю среду при экспираторных актах (кашель, чихание, активный разговор). Заражение происходит при вдохе образующегося воздушно-капельного аэрозоля. Допускается передача и через капельно-ядрышковую фазу аэрозоля. Высокая плотность людей в помещениях, длительное тесное общение являются условиями, благоприятствующими заражению. В организованных коллективах с круглосуточным пребыванием детей и взрослых воздушно-капельный путь передачи возбудителя наиболее эффективен в спальных помещениях, игровых комнатах, местах длительного пребывания членов коллектива. При этом следует учитывать, что на расстоянии более 3 м этот путь передачи практически не осуществляется.
Возбудитель чаще всего выделяется во внешнюю среду при экспираторных актах (кашель, чихание, активный разговор). Заражение происходит при вдохе образующегося воздушно-капельного аэрозоля. Допускается передача и через капельно-ядрышковую фазу аэрозоля. Высокая плотность людей в помещениях, длительное тесное общение являются условиями, благоприятствующими заражению. В организованных коллективах с круглосуточным пребыванием детей и взрослых воздушно-капельный путь передачи возбудителя наиболее эффективен в спальных помещениях, игровых комнатах, местах длительного пребывания членов коллектива. При этом следует учитывать, что на расстоянии более 3 м этот путь передачи практически не осуществляется.
Дополнительными факторами, способствующими передаче возбудителя, являются низкая температура и высокая влажность воздуха в помещении, так как в этих условиях дольше сохраняется капельная фаза аэрозоля, в которой возбудитель содержится в вирулентном состоянии.
Помимо аэрозольного, в передаче возбудителей инфекции определенную роль играют бытовой и алиментарный пути заражения. Факторами передачи возбудителя в первом случае являются загрязненные руки и предметы ухода, а во втором – инфицированная пища. СГА, попадая в определенные пищевые продукты, способны размножаться и длительно находиться в них в вирулентном состоянии. Описаны вспышки заболеваний ангиной или фарингитом при употреблении таких пищевых продуктов, как молоко, компоты, сливочное масло, салат из вареных яиц, омара, моллюсков, бутербродов с яйцом, ветчиной и др. Риску развития гнойных осложнений стрептококкового генеза подвергаются раненые, обожженные, больные в послеоперационном периоде, а также роженицы и новорожденные. Инфекция может развиться и эндогенным путем.
Естественная восприимчивость людей высока. В последние годы получены данные о связи между группами крови системы ABO, HLA-антигенами и аллоантигенами В-лимфоцитов D8/17 и заболеваниями ревматизмом, а также скарлатиной и ангиной.
Бета-гемолитические СГА наиболее вирулентны для человека. Они вызывают фарингит, тонзиллит, пневмонию. Кроме того, СГА являются этиологическим фактором развития скарлатины, кожных инфекций, ревматических осложнений и гломерулонефрита.
Бактериофаги – это современная альтернатива антибиотикам. Особенно в тех случаях, когда применение антибиотиков затруднено. Первый известный науке отчет об успешной фаготерапии был сделан в 1921 г. Брийонгом и Майсином, которые использовали стафилококковый бактериофаг для лечения заразных болезней кожи. В 1920-е гг. фаги активно использовались при лечении разных заболеваний [7–9]. Однако в 1940-е гг. они были потеснены антибиотиками, а на Западе о фагах забыли вовсе [10–14].

Сегодня в западных странах интерес к фагам проснулся вновь. Побудительным мотивом к этому явилось все возрастающее число устойчивых к антибиотикам микроорганизмов, особенно стафилококков и синегнойной палочки [6, 10].
Целью работы была оценка эпидемиологической эффективности применения бактериофагов (стрептококкового, стафилококкового, пиобактериофага поливалентного) для профилактики острых респираторных инфекций бактериальной этиологии в организованных коллективах в период их формирования.
Задачи исследования:
- Изучить уровень, структуру и динамику заболеваемости стрептококковыми инфекциями и БОД бактериальной этиологии в организованных коллективах военнослужащих.
- Изучить этиологическую структуру возбудителей БОД в организованных коллективах военнослужащих.
- Выявить группы военнослужащих, имеющих повышенный риск заболевания БОД бактериальной этиологии, а также факторы внешней среды, способствующие повышению заболеваемости у военнослужащих.
- Усовершенствовать систему эпидемиологического надзора за БОД в организованных коллективах военнослужащих.
- Оптимизировать систему мероприятий по профилактике стрептококковых инфекций с применением бактериофагов в организованных коллективах.
Материалы и методы
Оценку эффективности применения бактериофагов и бициллина-5 осуществляли по двум направлениям: микробиологическому и эпидемиологическому.
Микробиологические исследования (динамика изменения микробного пейзажа у военнослужащих основной и контрольной групп до и после применения профилактических средств) проводили в лаборатории 1026 центра государственного санитарно-эпидемиологического надзора Центрального военного округа Министерства обороны (Екатеринбург). Мазок из зева [15] для бактериологического исследования забирали до утреннего туалета полости рта, натощак в соответствии с требованиями методических указаний [16]. Количественные исследования мокроты проводили в соответствии с требованиями приказа Министерства здравоохранения СССР от 22.04.1985 г. № 535 [17]. Диагностически значимой считали концентрацию возбудителя 105 и выше в 1 мл бульона.
Специфичность (литическую активность) бактериофагов в отношении выделенных чистых культур определяли методом Отто (стекающей капли) путем добавления на питательные среды соответствующего бактериофага. В качестве контроля добавляли чистый физиологический раствор.
Эпидемиологическую эффективность применения бактериофагов (стрептококкового, стафилококкового, пиобактериофага поливалентного) и бициллина-5 оценивали путем анализа проявлений эпидемического процесса заболеваемости тонзиллитами (и другими БОД бактериальной этиологии) в опытной и контрольной группах до и после применения профилактических средств. Для анализа использовали схему когортного исследования, рекомендованного ВОЗ (WHO, 92324). Статистическую значимость различий показателей оценивали методом хи-квадрат (χ2), заполняя четырехпольную таблицу [18]. Статистически достоверными считали различия, при которых значение χ2 составляло более 3,841 (p ≤ 0,05).
В исследовании принимали участие 510 здоровых военнослужащих (мужчин), призванных в ВС РФ в декабре 2013 г. из 26 субъектов Приволжского, Уральского и Сибирского федеральных округов, в возрасте от 18 до 26 лет (средний возраст – 19,3 ± 1,6 года) и проходивших военную службу по призыву в одном из учебных воинских соединений на территории Свердловской области.
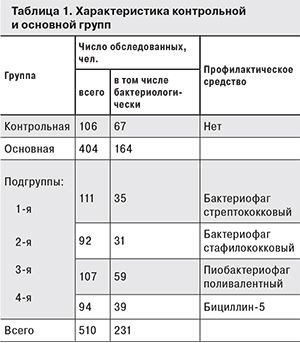
В процессе повседневной военно-профессиональной деятельности военнослужащие занимались учебно-боевой подготовкой в учебных классах и полевых условиях, обслуживанием военной техники в парке. Военнослужащие основной группы (п = 404) были распределены на 4 подгруппы по принципу принадлежности к воинскому подразделению (табл. 1).
 В 1-ю подгруппу вошли лица, получавшие с 14.01 по 03.02 2014 (3 календарные недели) бактериофаг стрептококковый, раствор для приема внутрь, местного и наружного применения (ФГУП «НПО «Микроген», Пермь).
В 1-ю подгруппу вошли лица, получавшие с 14.01 по 03.02 2014 (3 календарные недели) бактериофаг стрептококковый, раствор для приема внутрь, местного и наружного применения (ФГУП «НПО «Микроген», Пермь).
Во 2-ю подгруппу вошли лица, получавшие в этот же период бактериофаг стафилококковый, раствор для приема внутрь (ФГУП «НПО «Микроген», Нижний Новгород).
В 3-ю подгруппу вошли лица, получавшие в этот же период пиобактериофаг поливалентный (секстафаг), раствор для приема внутрь (ФГУП «НПО «Микроген», Пермь).
Все виды бактериофагов разводили в соотношении 1:1 с физиологическим раствором в условиях аптеки лечебного учреждения. Применяли все виды бактериофагов путем аэрозольного орошения ротоглотки по 1,5–2 мл, 2 раза в день (утром за 1,5 ч до приема пищи, вечером – через 2 ч после него).
В 4-ю подгруппу вошли лица, получившие однократно бициллин-5 (ОАО «Синтез», Курган).
В контрольную группу вошли 106 военнослужащих одного из подразделений учебного воинского соединения, имеющих аналогичные условия размещения, питания, труда, отдыха и военно-профессиональной деятельности, не получавших ни одного из перечисленных профилактических средств и прививок.
Результаты и обсуждение
Структура общей первичной заболеваемости военнослужащих учебного центра и в ВС РФ в целом представлена в табл. 2. В обоих случаях первое ранговое место занимают БОД, затем следуют болезни кожи и подкожной клетчатки, некоторые инфекционные и паразитарные болезни. На долю остальных 16 классов и нозоформ в учебном центре пришлось 12,3% заболеваний, в ВС РФ – 22,6%.
Уровень заболеваемости БОД военнослужащих учебного центра в 2014 г. составил 1749,42‰, что статистически достоверно превышает показатели заболеваемости в ВС РФ (723,00‰) и в Российской Федерации (333,70‰) в 2,4 и 5,2 раза соответственно (p < 0,05).
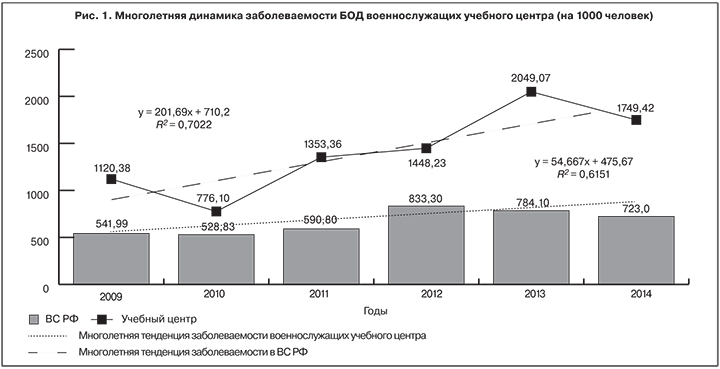
В многолетней динамике заболеваемости БОД (ОРЗ, острые тонзиллиты, внебольничные пневмонии, бронхиты и бронхиолиты) военнослужащих учебного центра (рис. 1) за период 2009–2014 гг. наметилась устойчивая тенденция к росту (коэффициент регрессии b составил +201,69, коэффициент детерминации R2 – 0,7022). В ВС РФ за этот же период также наметилась тенденция к росту, но менее выраженная (b = +54,67, R2 = 0,62).
Наименьший уровень заболеваемости БОД военнослужащих как учебного центра, так и ВС РФ был зарегистрировн в 2010 г. – 776,10 и 528,83‰ соответственно. Наибольший уровень зарегистрирован в учебном центре в 2013 г. (2049,07‰), в ВС РФ – в 2012 г. (833,30‰). На протяжении всего изучаемого периода уровень заболеваемости БОД военнослужащих учебного центра превышал показатели в ВС РФ от 1,5 (в 2010 г.) до 2,6 раз (в 2013 г.).
В 2014 г. в структуре БОД военнослужащих как учебного центра (рис. 2), так и ВС РФ преобладают ОРЗ: 62,0 и 61,7% соответственно.
Заболеваемость другими стрептококковыми инфекциями и заболеваниями, такими как рожа, гломерулонефрит, ревматические осложнения, в ВС РФ носит спорадический характер и в учебном центре первостепенного эпидемиологического значения не имеет.
Учитывая преимущественно осенне-зимнюю сезонность стрептококковых инфекций и БОД бактериальной этиологии, при построении графиков внутригодовой динамики заболеваемости военнослужащих учебного центра использовали эпидемический год, начинающийся с 1 июня и заканчивающийся 31 мая следующего года.
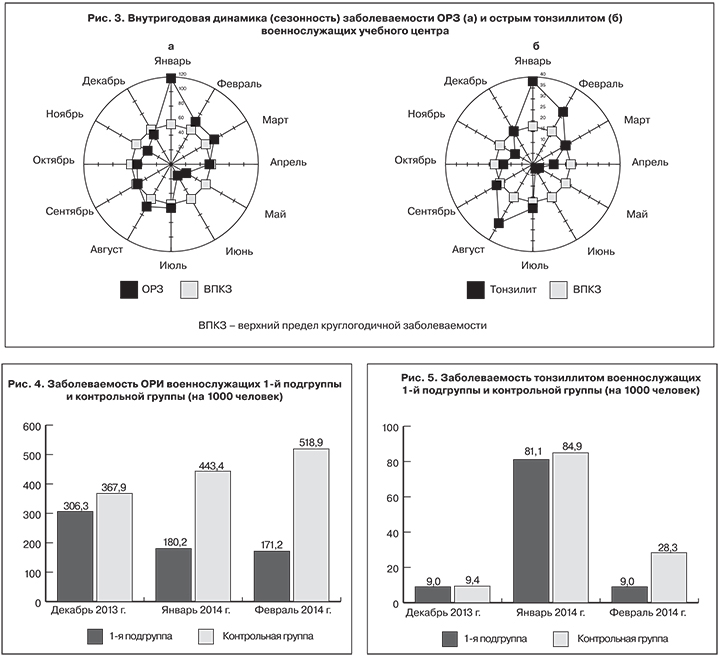
Внутригодовая динамика заболеваемости ОРЗ (рис. 3) военнослужащих учебного центра соответствует четырем фаза развития эпидемического процесса. В течение года наблюдаются 2 сезонных подъема, превышающих верхний предел круглогодичной заболеваемости (55,08‰). Меньший – летний (июль–август), бóльший – зимний (декабрь–март). Пик заболеваемости ОРЗ приходится на январь (118,26‰).
Сезонная заболеваемость острым тонзиллитом (так же как и другими БОД) в учебном центре определяется временем прибытия пополнения, то есть периодом начального перемешивания личного состава с разным уровнем иммунитета к сложившейся в коллективе или занесенной в него стрептококковой микрофлоре. При этом в зависимости от внутренних особенностей воинских подразделений (доля новобранцев, условия размещения военнослужащих в казармах, длительность пребывания их в закрытых помещениях) повышение заболеваемости тонзиллитом начинается в первые же дни после прибытия пополнения, достигая максимума через 1,5–2 мес.
Бактериофаг стрептококковый. В структуре выделенных культур (до применения бактериофага стрептококкового) преобладали стрептококки (табл. 3).
После профилактического курса количество выделенных стрептококков в 1-й подгруппе уменьшилось в 2,4 раза в основном за счет уменьшения доли пневмококков, а в контрольной группе увеличилось в 2,8 раза за счет роста доли стрептококков и появления пневмококков.
Исходные уровни заболеваемости ОРИ бактериальной этиологии в 1-й подгруппе и контрольной группе) статистически достоверно не различались, составляя 306,3 и 367,9‰ соответственно (χ2 = 0,67; p > 0,05) (рис. 4).
К окончанию исследования показатель заболеваемости ОРИ в 1-й подгруппе достоверно снизился в 1,8 раза (χ2 = 4,86; p < 0,05), а в контрольной группе он вырос в 1,4 раза (χ2 = 4,30; p < 0,05). После профилактического курса стрептококкового бактериофага уровень заболеваемости в 1-й подгруппе был в 3,0 раза ниже, чем в контрольной группе (χ2 = 27,64; p < 0,05).
Исходные уровени заболеваемости тонзиллитом в 1-й подгруппе и контрольной группе также статистически достоверно не различались и составляли 9,0 и 9,4‰ соответственно (χ2 = 0,45; p > 0,05) (рис. 5).
Во время проведения профилактического курса (январь 2014 г.) уровень заболеваемости тонзиллитом в 1-й подгруппе вырос в 9,0 раз (χ2 = 5,13; p < 0,05). Аналогичный рост заболеваемости (в 9,0 раз) в этот же период наблюдался и в контрольной группе (χ2 = 5,14; p < 0,05).
Однако после завершения профилактического курса уровень заболеваемости в 1-й подгруппе достоверно снизился до исходного уровня (χ2 = 5,13; p < 0,05), а в контрольной группе – только в 3 раза, при этом статистической достоверности различий не выявлено (χ2 = 2,2; p > 0,05).
Эффективность в снижении заболеваемости тонзиллитом связана со стрептококковой этиологией заболеваний. Высокую эффективность бактериофага стрептококкового в отношении S. рneumoniaе подтверждает отсутствие даже спорадических случаев заболеваний нижних дыхательных путей (бронхита, пневмонии) в 1-й подгруппе, хотя до применения бактериофага такие заболевания регистрировались.
Случаев заболевания скарлатиной в 1-й подгруппе и контрольной группе в период исследования не зарегистрировано.
Бактериофаг стафилококковый. Во 2-й подгруппе исходно в структуре выделенных культур преобладали стрептококки. Они были выделены у 23 (71,9%) человек: S. pneumoniae – у 5 (15,6%), S. pyogenes – у 18 (56,3%). S. aureus выделялись у 9 (28,1%) человек. В контрольной группе результаты оказались схожими: стрептококки были выделены у 13 (76,5%) человек, S. aureus – у 4 (23,5%).
После профилактического курса количество выделенных стафилококков во 2-й подгруппе уменьшилось в 1,8 раза, при этом статистической достоверности не выявлено (χ2 = 0,03; p > 0,05). Однако выявлено комбинированное носительство S. pneumoniae и S. aureus (8,2%). В контрольной группе количество выделенных культур стафилококков уменьшилось (χ2 = 12,54; p < 0,05).
Динамика заболеваемости ОРИ во 2-й подгруппе после профилактического курса стафилококкового бактериофага свидетельствует о достоверном снижении в 1,7 раза. В то же время отмечена более низкая эффективность бактериофага стафилококкового в снижении заболеваемости тонзиллитом, что связано с преимущественно стрептококковой этиологией заболевания.
Бактериофаг поливалентный (секстафаг). В 3-й подгруппе исходно у 12 (75,0%) человек были выделены стрептококки и у 4 (25,0%) – S. aureus. В контрольной группе стрептококки выделены у 13 (76,5%) человек, S. aureus – у 4 (в 23,5%).
После профилактического курса у 8 военнослужащих выделен S. pneumoniae. Других возбудителей и их комбинаций выделено не было.
Динамика заболеваемости военнослужащих ОРИ в 3-й подгруппе После профилактического курса полибактериофага произошло незначительное, статистически не значимое снижение заболеваемости. При этом в контрольной группе уровень заболеваемости вырос в 1,4 раза.
Бициллин-5. В 4-й подгруппе до применения бициллина-5 и после его однократного введения в структуре выделенных культур статистически достоверных различий не выявлено. Однако исследования показали высокую чувствительность выделенных культур S. pyogenes к антибиотикам пенициллинового ряда, в том числе к бициллину-5.
Выводы
- В структуре общей первичной заболеваемости в организованных воинских коллективах доля БОД составляет до 70%.
- В структуре этиологических агентов острых респираторных инфекций в организованных коллективах военнослужащих преобладают S. pneumoniae и S. pyogenes (до 75%) и S. aureus (20–25%).
- Основной группой риска заболевания острыми респираторными инфекциями являются военнослужащие из числа молодого пополнения, они составляют 65–80% численного состава подразделений учебного типа. Наиболее значимыми факторами риска, способствующими повышению заболеваемости БОД в организованном коллективе, являются: несоблюдение требований, предъявляемых к размещению (скученность); общее переохлаждение организма в результате неблагоприятного воздействия комплекса метеорологических факторов; нарушение качественной и количественной адекватности питания; переутомление.
- Профилактическое применение бактериофага стрептококкового в период формирования воинского коллектива позволило достоверно снизить уровень заболеваемости военнослужащих ОРИ бактериальной этиологии в 1,8 раза, тонзиллитами – в 9,0 раз. Высокая эффективность препарата связана с преимущественно стрептококковой этиологией этих заболеваний.
- Высокая эффективность бактериофагов в снижении уровня заболеваемости тонзиллитами и более длительный профилактический эффект по сравнению с результатом, полученным при применении бициллина-5, подтверждает предпочтительность их применения в воинских коллективах.
- Применение бактериофагов не влияет на проведение плановой иммунопрофилактики военнослужащих в период формирования воинских коллективов, может применяться как отдельно, так и в сочетании с антибиотиками и не оказывает негативного влияния на иммунный статус лиц призывного возраста.
При применении бактериофагов для профилактики простудной заболеваемости отмечается эффект санации организованного воинского коллектива. В результате местного действия на микрофлору носоглотки нарушается процесс циркуляция в коллективе возбудителей простудных заболеваний кокковой этиологии и, как следствие, предотвращается формирование эпидемического штамма, обусловливающего групповую заболеваемость. - Применение бактериофагов путем аэрозольного орошения ротоглотки в течение трех календарных недель не вызывает аллергических реакций.
- Применение бактериофагов является современным направлением профилактики инфекционных болезней стрептококковой этиологии в организованных коллективах военнослужащих.


