Значительные успехи в терапии ВИЧ-инфекции, которые привели к снижению смертности от этого заболевания, были достигнуты после внедрения высокоактивной антиретровирусной терапии. Терапевтический успех любого лечения зависит не только от свойств лекарственного препарата, но и от способности пациента следовать назначенному режиму терапии. Это особенно важно в отношении ВИЧ-инфекции, при которой главной целью лечения является полное подавление репликации вируса и улучшение иммунных показателей. Приверженность к терапии является основным фактором достижения эффективности и успешной профилактики развития резистентности ВИЧ. Риск вирусологической неудачи существенно возрастает при снижении приверженности менее 95% (т.е. пропуске 1 дозы или 1 дня лечения в месяц). Приверженность менее 70% ставит под угрозу эффективность практически всех антиретровирусных препаратов (АРВП) [1, 2]. Существует ряд факторов, способных повлиять на приверженность и, в конечном итоге, на эффективность антиретровирусной терапии (АРВТ). Помимо индивидуальной переносимости препаратов, существуют как субъективные факторы (низкий уровень психологического компонента: боязнь раскрытия диагноза, страх приема АРВТ, ощущение влияния на повседневную жизнь и т.д.), так и объективные (требования к диете, частота приема, количество таблеток, соблюдение времени приема, ошибки в дозировке) [3–6]. Создание препаратов с фиксированными комбинациями доз (ФКД) позволило добиться повышения приверженности путем воздействия на объективные факторы. Режимы фиксированных доз включают в себя 2 и более лекарственных компонента с синергическим действием, соединенных в одной лекарственной форме в фиксированных пропорциях, при этом доза отдельных компонентов является биоэквивалентной.
Проведенный мета-анализ 9 рандомизированных клинических исследований с участием 20 242 пациентов с различными заболеваниями (артериальная гипертензия – 4 больных, сахарный диабет – 2, туберкулез – 2 и ВИЧ-инфекция – 1) показал снижение вероятности несоблюдения назначений на 26% при использовании лекарственных средств в ФКД по сравнению с применением тех же препаратов в виде отдельных компонентов [7].
Анализ данных 76 исследований по целому ряду медицинских специальностей, в которых проводился электронный мониторинг приверженности к лечению, показал, что при однократном дозировании средняя приверженность к приему разовой дозы составляет 79%, а при двукратном – 69%, приверженность ко времени приема – 74 и 58% соответственно [8].
Однако ВИЧ-инфекция отличается от многих заболеваний тем, что АРВТ должна проводиться пожизненно. Для оценки влияния частоты дозирования АРВП на соблюдение режима лечения в 2009 г. был проведен мета-анализ 11 клинических исследований, включавших 3029 пациентов с ВИЧ-инфекцией. Частота достижения вирусологического ответа и приверженность к лечению в случае однократного приема АРВП была достоверно выше, чем при приеме 2 раза в сутки (p = 0,003) [9]. Больные отдавали предпочтение схемам лечения, предусматривающим прием наименьшего количества таблеток 1 раз в сутки. Однако это не касалось пациентов, долгое время находящихся на АРВТ. Вероятно, у таких больных главную роль играет «усталость от терапии» и снижение приверженности в целом, при этом кратность приема препаратов уже оказывает существенно меньшее влияние на вирусологическую эффективность.
По нашим наблюдениям, достаточно часто встречаются ситуации, когда уменьшение количества таблеток и кратности их приема может существенно улучшить приверженность к лечению и поддерживать вирусологический ответ даже у пациентов, долгое время находящихся на АРВТ. В качестве примера приведем случай с больным Л.
Пациент Л., 49 лет, руководитель собственной компании, часто выезжает в командировки. В 2005 г. была диагностирована ВИЧ-инфекция, стадия 4А. Заражение произошло при незащищенном гетеросексуальном контакте с неизвестной партнершей. При постановке диагноза уровень РНК ВИЧ в плазме крови составил 86 700 копий/мл, количество CD4+-лимфоцитов – 181 клеток/мкл (17%), содержание гемоглобина (Hb) – 149 г/л, аланинаминотрансферазы (АЛТ) – 26 МЕ/л, аспартатаминотрансферазы (АСТ) – 23 МЕ/л.
Маркеры вирусных гепатитов (HbsAg, aнти-HCV, анти-HBc) не выявлены, ПЦР на ЦМВ, HCV – отрицательная, криптококковый антиген – отсутствует, RW – отрицательная. Флюрография, УЗИ брюшной полости без патологии. Сопутствующее заболевание: ожирение 1–2-й степени (вес – 121 кг). Наследственность: инфаркт миокарда у отца в возрасте 45 лет. При осмотре: кандидоз слизистых оболочек полости рта.
Учитывая низкий иммунный статус, ожирение, наследственность и образ жизни пациента, была назначена схема EFV (эфавиренз)+ AZT /3TC (зидовудин/ламивудин – комбивир). Для лечения кандидоза ротоглотки назначен флюконазол, для профилактики пневмоцистной пневмонии – бисептол.
Через 1 мес. от начала АРВТ содержание Нb уменьшилось до 105 г/л, а через 3 мес. – до 92 г/л. Кроме того, пациент жаловался на выраженное головокружение и плохой сон, а также невозможность сосредоточиться на работе. Уровень РНК ВИЧ в плазме крови был ниже порога определения (< 40 копий/мл), количество CD4+-лимфоцитов составило 276 клеток/мкл (19%).
Ввиду недоступности препарата кивекса (на тот момент он не был зарегистрирован в РФ) было решено поменять всю схему на ATV (атазанавир, 400 мг) + ABC (абакавир) + 3TC в виде монопрепаратов (всего 6 таблеток, двукратный прием). Через 1 мес. терапии по новой схеме содержание Нb восстановилось до 128 г/л, нежелательных явлений (НЯ) или проявлений реакции гиперчувствительности (РГЧ) не было отмечено. Через 1 год больного беспокоит неудобство, связанное с большим количеством таблеток и приемом препаратов 2 раза в сутки. Он сообщил, что примерно 1–2 раза в месяц забывает принять вовремя лекарства из-за деловых встреч. При этом вирусологическая и иммунологическая эффективность сохранялась.
Для упрощения схемы лечения ABC + 3TC заменили комбинированным препаратом кивекса, доступным в Центре по профилактике и борьбе со СПИДом. Пациент уже более 5 лет принимает назначенную схему, выражая удовлетворенность лечением. У больного достигнута стойкая вирусологическая супрессия (< 40 копий/мл) и иммунологическая эффективность (583 клеток/мкл, 35%).
J.D. Willing и соавт. [10] выдвинули гипотезу о том, что современные АРВП (в особенности ФКД), обеспечивая лучшую переносимость и удобство, могут способствовать большей продолжительности пребывания на одной линии терапии. Ретроспективный анализ данных пациентов, начавших терапию до 2000 г. (n = 293; отсутствие ФКД), в период 2000–2004 гг. (n = 309; появление первых ФКД) и в 2004–2007 гг. (n = 233; ФКД с однократным режимом приема), подтвердил это предположение. Была выявлена статистически достоверная зависимость продолжительности терапии от характеристик режимов (препараты, частота приема, количество таблеток). Сравнивали длительность пребывания на первой линии терапии пациентов, получавших 6 и более таблеток в день (n = 67), 4–5 таблеток в день (n =117), 3 и менее таблеток в день (n = 358). Больные, принимавшие 3 и менее таблеток в день, находились на первой линии терапии наиболее продолжительное время – в среднем 1218 дней (в сравнении с 766 днями при приеме 4–5 таблеток и 340 днями для 6 и более таблеток). Кроме того, сравнивали продолжительность первой линии АРВТ у пациентов, получавших однократный режим терапии (n = 228), и пациентов, получавших дву- и более кратный режим (n = 314). Схемы с приемом 1 раз в день имели преимущество по продолжительности лечения (1253 дня по сравнению с 712 днями для схем с большей кратностью приемов).
В настоящее время в России зарегистрировано несколько комбинированных препаратов, включающих 2 или 3 нуклеозидных ингибитора обратной транскриптазы (НИОТ), в том числе комбивир (AZT) + 3TC), кивекса (3TC + ABC), тризивир [зидовудин (AZT) + 3TC + ABC] и трувада [тенофовир (TDF) + эмтрицитабин (FTC)], но однократный прием одобрен только для кивексы и трувады, поэтому Европейские рекомендации, рекомендации США, международного общества по изучению СПИД отдают им предпочтение [11, 12].
Сочетание ABC и 3TC в виде отдельных компонентов давно зарекомендовало себя наилучшим образом. Так, в исследовании CNA 30024 по сравнению ABC + 3TC (2 раза в сутки) + EFV с AZT + 3TC (2 раза в сутки) + EFV показана равная вирусологическая эффективность схем независимо от исходного уровня РНК ВИЧ (больше или меньше 100 000 копий/мл) и больший прирост числа CD4+-лимфоцитов у больных, получавших АВС (209 и 155 клеток/мкл; p = 0,0039), а также лучшие переносимость и профиль безопасности абакавирсодержащего режима [13].
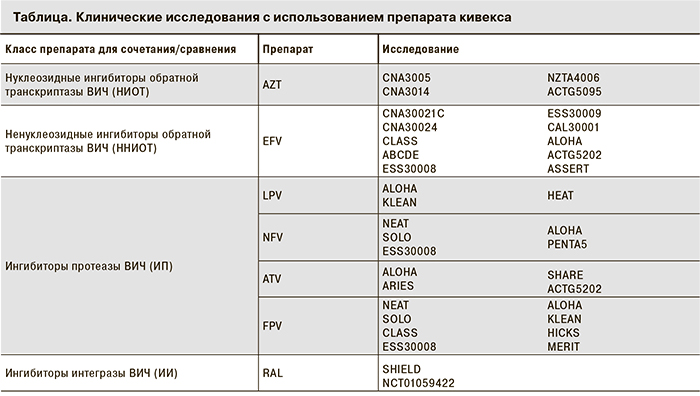
Эффективность и безопасность препарата кивекса в виде ФКД подтверждена многочисленными клиническими исследованиями и не зависит от третьего компонента схемы АРВТ (см. таблицу).
В последние годы было проведено несколько крупных международных рандомизированных исследований, в которых сравнивали две фиксированные комбинации НИОТ с однократным приемом в сутки – препараты кивекса (ABC/3TC) и трувада (TDF/FTC) (HEAT, ASSERT, ACTG 5202 для пациентов, ранее не получавших АРВТ, и BICOMBO, STEAL, SWIFT – для больных, имевших опыт использования АРВП) [14–19]. В большинстве исследований эффективность двух фиксированных комбинаций была одинаковой, хотя некоторыми специалистами были получены противоречивые данные по сравнительной эффективности абакавирсодержащих и тенофовирсодержащих режимов у пациентов с исходно высокой вирусной нагрузкой. Объединенный анализ результатов этих исследований не подтвердил опасений по поводу меньшей эффективности у этой категории больных [20].
Важным аспектом при выборе схемы АРВТ также является безопасность АРВП. С этой точки зрения сочетание АВС и 3ТС (в том числе и в виде ФКД) по многим параметрам превосходит наиболее часто используемый в России комбинированный препарат комбивир (AZT + 3TC). Это касается, прежде всего, частоты развития анемии и нейтропении, нарушений липидного обмена, в том числе липодистрофии, а также симптомов со стороны желудочно-кишечного тракта. Основные преимущества ФКД ABC/3TC перед TDF/FTC заключаются в минимальном влиянии на функцию почек и состояние костной ткани пациента.
К несомненным достоинствам препарата кивекса относят прием 1 таблетки 1 раз в сутки независимо от пищевого режима. Гипотеза об улучшении приверженности при назначении ABC/3TC по сравнению с монокомпонентами была подтверждена рядом исследований. В исследовании SEAL (ESS30008) принимали участие 260 пациентов, исходно получавших не менее 6 мес. АРВТ, включавшую ABC, 3TC и ИП или ННИОТ. Больные были рандомизированы в равном соотношении (1:1) в группы 48-недельного приема ABC/3TC 1 раз в сутки или продолжения приема отдельных компонентов (ABC и 3TC) 2 раза в сутки [21]. Первичными конечными точками были частота вирусологической неудачи и НЯ 2–4-й степени, вторичными точками – процент больных с неопределяемой РНК ВИЧ, изменение количества CD4+-клеток от исходного, время до клинического прогрессирования заболевания или смерти, приверженность к лечению и развитие генотипической резистентности в случае вирусологической неудачи. Исходные характеристики были сопоставимы в обеих группах. Исследование завершили 92 и 90% респондентов в каждой группе соответственно. Вирусологическая неудача встречалась редко (2,3%) и была связана с появлением мутаций резистентности у 2 больных из группы кивексы и у 4 больных из группы монокомпонентов. Частота НЯ 2–4-й степени была низкой и сопоставимой между группами лечения. Кроме того, ни один больной не прервал АРВТ из-за связанных с лечением НЯ, не связанных с лечением серьезных НЯ или смерти. В данном исследовании не было ни одного случая гиперчувствительности к АВС. Медиана приверженности составила 93% в обеих группах, что позволило добиться вирусологической супрессии у 81 и 82% пациентов (ITT-анализ) в группе кивексы и в группе монокомпонентов соответственно. Доля пациентов, имевших высокий (> 95%) уровень приверженности, обеспечивающий оптимальную вирусологическую супрессию вируса, была выше в группе пациентов, получавших кивексу (39% по сравнению с 31% в группе получавших ABC + 3TC).
В рандомизированном 8-недельном исследовании D. Maitland и соавт. [22] изучали переключение 94 пациентов со стабильной вирусологической супрессией, получавших отдельно ABC и 3TC дважды в день в сочетании с любым третьим АРВП, на кивексу с однократным приемом. При этом в первые 4 нед. половине больных была назначена кивекса (1-я группа), а оставшиеся пациенты продолжили раздельный прием исследуемых препаратов (2-я группа). В последующие 4 недели все пациенты были переведены на однократный прием кивексы. Обычно для оценки приверженности используют метод подсчета таблеток. В описываемом исследовании применяли потенциально более точный метод – контейнеры для таблеток с системой контроля открытия (MEMS). В данное устройство встроен микрочип, позволяющий фиксировать каждое открытие контейнера и записывать его дату и время. Оценивали 3 показателя: общую приверженность, приверженность к дозе (процент дней с правильно принятым числом доз препаратов) и приверженность ко времени приема (процент доз, принятых с интервалом + 3 ч от предписанного времени). Кроме того, больные заполняли опросник удовлетворенности лечением (HIVTSQ) и шкалы тревоги и депрессии (HADS). Группы были хорошо сбалансированы по исходным параметрам (полу, возрасту, расе, иммунному статусу). Большинство больных в качестве третьего препарата получали ЕFV или невирапин (NVP). Результаты исследования продемонстрировали, что упрощение режима существенно увеличивает приверженность к лечению. Так, общая приверженность в 1-й и 2-й группах составила 99,2 и 96,6% (p = 0,017), приверженность к дозе – 97,1 и 91,9% (p = 0,016), приверженность ко времени – 95,5 и 86,3% (p = 0,006). Удовлетворенность лечением также была значительно выше в группе с однократным приемом кивексы (92 и 85%; p = 0,004). Лишь 2 пациента вернулись к раздельному приему препаратов из-за непереносимости кивексы (головная боль и тошнота).
В реальной клинической практике различия по приверженности к лечению препаратами в форме ФКД 1 раз в день и монокомпонентами могут быть существенны, так как в клинических исследованиях с пациентами проводится большая работа по соблюдению режима АРВТ, и хорошие результаты получаются даже при двукратном дозировании и большем количестве таблеток. Это предположение подтверждено когортными ретроспективными исследованиями по анализу баз данных пациентов, получавших нуклеозидную основу AZT + 3TC. У больных, использовавших ФКД AZT/3TC, приверженность была в 2–3 раза лучше, чем у пациентов, использовавших AZT + 3TC в виде монокомпонентов [23, 24].
Результаты еще одного когортного ретроспективного исследования по сравнению приверженности к АРВТ на основе кивексы (группа ФКД) и монопрепаратов ABC и 3TC (группа НИОТ Combo) были опубликованы T.L. Kauf и соавт. в 2012 г. [25]. Авторы использовали базу данных системы здравоохранения США, которая включала информацию о 38 млн пациентов, которым была оказана любая медицинская помощь с 1997 по 2005 г. После соблюдения критериев включения и исключения группа ФКД составила 650 человек, а группа раздельного использования соответствующих препаратов – 1947 человек. В обеих группах пропорции пациентов, получавших ННИОТ или ИП в качестве третьего препарата, были сходными. Продолжительность наблюдения за группой ФКД составила 272 дня, за группой НИОТ Combo – 338 дней. Возраст большинства больных находился в пределах 35–54 лет, мужчины составляли 82,7%. Медиана приверженности в группе ФКД составила 96% по сравнению с 89% в группе НИОТ Combo (p < 0,0001). Но уникальность этого исследования состоит в том, что используемые в нем статистические методы позволили подсчитать приверженность не только к лечению препаратами кивекса, АВС и 3ТС, но и к третьему компоненту схемы в зависимости от нуклеозидной основы. Так, средняя приверженность к третьему компоненту режима АРВТ составила 92,3 и 85% в двух группах соответственно (p < 0,0001). Мультивариантный логистический регрессионный анализ показал, что больные из группы ФКД имели на 48% больше шансов для соблюдения 95-процентного уровня приверженности к третьему компоненту по сравнению с группой НИОТ Combo и на 39% больше – для соблюдения 90-процентной приверженности (p < 0,03).
Основным ограничением приема абакавирсодержащего режима является развитие РГЧ, которая связана с наличием генетического аллеля HLA-B*5701. В России частота встречаемости HLA-B*5701 среди ВИЧ-инфицированных лиц составляет 4,1%. Перед назначением пациенту АВС в составе АРВТ целесообразно провести исследование на наличие аллеля HLA-B*5701 для минимизации риска развития РГЧ (отрицательный результат имеет близкую к 100% предсказательную ценность). Безопасность и переносимость кивексы и монокомпонентов сопоставима, в том числе по частоте развития РГЧ [26].
Доступность скрининга на аллель HLA-B*5701 позволяет практически полностью исключить вероятность развития РГЧ к АВС. Несмотря на результат скрининга, клиническое наблюдение – самое лучшее средство профилактики развития РГЧ. Как правило, диагностика состояния не является существенной проблемой для врачей-инфекционистов, имеющих опыт применения АВС.
ФКД дают специалистам возможность более эффективного ведения хронических заболеваний, требующих пожизненной терапии, особенно это касается сочетанных заболеваний, требующих одновременного лечения (оппортунистические инфекции, туберкулез, хронические вирусные гепатиты и т. д.). Иногда количество принимаемых таблеток может составлять 15–18 в сутки, а кратность приема – до 4–6 раз в сутки, что существенно повышает риск несоблюдения врачебных назначений. Так, по результатам оценки приверженности к АРВТ Магнитогорским благотворительным фондом «Гражданская инициатива», у 239 пациентов, живущих с ВИЧ, в 26% случаев нарушения режима зависели от наличия сопутствующих заболеваний и необходимости приема большого количества лекарств помимо АРВТ [27].
Пациентка А., 25 лет, работает менеджером, ведет активный образ жизни, ходит в ночные клубы. Диагноз ВИЧ-инфекции поставлен в 2004 г. (ВИЧ-инфекция, стадия 3). Вероятное заражение произошло в 2001–2002 гг. при внутривенном введении психоактивных веществ. При постановке диагноза РНК ВИЧ в крови – 65 400 копий/мл, уровень CD4+-лимфоцитов – 434 клетки/мкл (21%), содержание Hb – 123 г/л, АЛТ – 45 МЕ/л, АСТ – 37 МЕ/л.
Маркеры вирусных гепатитов HbsAg и анти-HBc не выявлены, aнти-HCV – «+», ПЦР РНК HCV – положительная, RW – отрицательная. Флюрография, УЗИ брюшной полости – без патологии. Сопутствующее заболевание: хронический гепатит С (ХГС).
Пациентка отказалась начать лечение ХГС, АРВТ на тот момент не была показана.
В 2005 г. количество CD4+-лимфоцитов снизилось до 340 клеток/мкл (20%), РНК ВИЧ – 72 000 копий/мл. Была начата терапия по схеме EFV + AZT/3TC (комбивир). Больная хорошо переносила лечение, НЯ не было, за исключением снижения количества Нb 1-й степени.
Через 15 мес. АРВТ РНК ВИЧ < 40 копий/мл, CD4+-лимфоциты – 467 клеток/мкл (24%), Hb – 110 г/л, АЛТ – 63 МЕ/л, АСТ – 48 МЕ/л, РНК HCV – 3,8 х 106 копий/мл, генотип HCV – 3а. С пациенткой проведена беседа о необходимости лечения ХГС. Для предотвращения развития выраженной анемии в процессе противовирусной терапии ХГС комбивир был заменен на ABC + 3TC (зиаген + эпивир). Переносимость схемы хорошая. Через 2 мес. начата противовирусная терапия пегинтерфероном и рибавирином. С учетом противовирусной терапии ХГС больная получала 10 таблеток в сутки и 1 инъекцию пегинтерферона в неделю. Быстрого вирусологического ответа на 4-й неделе терапии получено не было. После беседы с пациенткой по соблюдению назначений выяснилось, что она часто пропускает прием всех лекарственных препаратов, чтобы уменьшить количество таблеток (чаще всего были избирательные неодновременные пропуски приема АВС, 3ТС и рибавирина). Больная считала, что «если не выпить 1–2 раза в неделю 1 таблетку какого-нибудь препарата», то это не отразится на эффективности лечения. Через месяц после беседы с лечащим врачом приверженность улучшилась, но была ниже 95%, так как пациентка иногда забывала принимать препараты.
Для повышения приверженности, упрощения схемы лечения и повышения вероятности достижения устойчивого вирусологического ответа на лечение ХГС ABC + 3TC заменили комбинированным препаратом кивекса. Пациентка достигла раннего вирусологического ответа на 12-й неделе лечения ХГС и смогла продолжить терапию до 48-й недели. В настоящее время больная принимает назначенную схему АРВТ (2 таблетки в сутки однократно), достигнут устойчивый вирусологический ответ на лечение ХГС, стойкая супрессия РНК ВИЧ (< 40 копий/мл) и иммунологическая эффективность (543 клеток/мкл; 32%).
Таким образом, успешная терапия и долгосрочный контроль репликации ВИЧ требют высокого уровня соблюдения режима лечения. Представленные данные позволяют применять препарат кивекса не только для первой линии терапии, но и для переключения с других НИОТ для упрощения режима лечения без потери вирусологической эффективности и риска увеличения токсичности. Кивекса может сочетаться как с ННИОТ, так и с ИП и ИИ. Для удобства пациентов и повышения приверженности ФКД с однократным приемом включены в предпочтительный режим большинства современных рекомендаций, в том числе в рекомендации российского Национального научного общества инфекционистов [28]. ФКД представляют важный шаг вперед в лечении ВИЧ-инфекции за счет снижения лекарственной нагрузки и частоты приема АРВП в долгосрочной перспективе.


