Глобальное бремя сахарного диабета (СД) оценивается Международной диабетической федерацией (IDF) в 382 млн человек (2013), что составляет 8,3% мирового населения. В России предположительная распространенность сахарного диабета – 7,6 %, а численность больных – 10,9 млн человек (2013), однако стоит учитывать, что гиподиагностика СД в России и в мире в среднем составляет около 46%. Это означает, что 175 млн человек в мире, живущих с СД, не знают об этом. Каждый год число больных СД возрастает на 5–7%, а каждые 10–15 лет удваивается. Так, по оценкам ВОЗ и IDF, к 2035 г. в мире будет 592 млн человек, страдающих СД, то есть рост числа заболевших составит 55% от количества больных в 2013 г. Осложнения СД и инвалидизация больных обусловливают высокие затраты на медицинское обеспечение таких пациентов. Достаточно высок уровень смертности в этой группе больных. Так, в 2013 г. в мире от осложнений СД умерло около 5,1 млн человек. К 2030 г., по оценкам ВОЗ, СД займет 7-ю позицию среди главных причин смертности. Общие расходы мирового здравоохранения на больных СД в 2013 г. составили 548 млрд долларов США. Дополнительный вклад в социальную значимость этой нозологии вносят женщины, страдающие гестационным СД, и беременные, которым диагноз диабета был поставлен до наступления беременности. В 2013 г. в мире было зарегистрировано около 21 млн беременных, страдающих гипергликемией, то есть каждые 6-е роды в 2013 г. проходили у женщины с нарушением углеводного обмена во время беременности.
Всем категориям больных, страдающих СД, необходим постоянный контроль гликемии. Исследование содержания глюкозы в капиллярной крови (ГКК) проводится для оценки эффективности гипогликемической терапии в рамках рутинного самоконтроля либо при измерении ГКК с помощью медперсонала у постели больного. Эта процедура является ценным диагностическим тестом для недопущения и своевременной диагностики гипогликемических состояний у больных СД в условиях эндокринологических центров (клиник), а также проводится повсеместно в отделениях терапевтического и хирургического профиля, отделениях реанимации и интенсивной терапии (ОРИТ) и других.
Способы измерения глюкозы можно подразделить на три группы: лабораторные измерения, исследования по месту лечения (ИМЛ-измерения), и измерения, самостоятельно выполняемые пациентами [1].
 Лабораторные измерения:
Лабораторные измерения:
- выполняются в условиях клинико-диагностической лаборатории (КДЛ) медицинскими работниками, имеющими специализацию в области лабораторной диагностики;
- для этих измерений применяют стационарное лабораторное оборудование, например, автоматические и полуавтоматические анализаторы глюкозы;
- как правило, лабораторные измерения территориально удалены от пациента и чаще бывают плановыми, но могут быть и экстренными (например, в экспресс-КДЛ) [1].
Еще одним экспресс-методом оценки уровня гликемии является анализ на содержание ГКК с помощью портативного глюкометра. Данный способ измерения концентрации глюкозы в крови является быстрым и удобным как для обследуемого, так и для врача. Результаты, полученные в ходе измерения, могут быть немедленно приняты во внимание и, при необходимости, могут быть внесены соответствующие коррективы.
Примерный перечень организаций, где может проводиться экспресс-контроль гликемии с помощью портативного глюкометра:
1. Медицинские организации:
- больницы;
- амбулаторные клиники.
2. Учреждения медико-социального обслуживания пожилых людей:
- дома престарелых с медицинским обслуживанием;
- дома престарелых с медицинским и бытовым уходом;
- дома-интернаты для престарелых и инвалидов.
3. Тюрьмы.
4. Учреждения (или организации), осуществляющие социально-медицинское обслуживание на дому, в том числе больницы скорой медицинской помощи.
5. Медицинские кабинеты учреждений системы социальной защиты населения:
- детские дома;
- приюты.
6. Медицинские кабинеты организаций отдыха и оздоровления детей:
- загородные оздоровительные лагеря;
- лагеря дневного пребывания;
- оздоровительные центры, базы и комплексы.
7. Медицинские кабинеты в школах.
Экспресс-контроль гликемии с помощью портативного глюкометра может также проводится при осуществлении услуг врачей частной практики.
По самым скромным подсчетам в России ежегодно производится около 1 млрд анализов на глюкозу, включая профессиональные измерения в медицинских учреждениях и самостоятельные измерения больными СД. Среди профессиональных измерений важнейшее место занимают ИМЛ [1]. ИМЛ-измерения глюкозы можно определить так [1]:
- выполняются в стационарных и амбулаторных медицинских учреждениях, а также при оказании медицинской помощи вне медицинского учреждения (например, бригадой скорой помощи);
- необходимы, когда требуется срочно получить результат измерения, а времени на отправку пробы в КДЛ нет;
- могут выполняться как специалистами в области лабораторной диагностики, так и медицинскими работниками другого профиля (например, врачом поликлиники или операционной сестрой), обученными обращению со средствами ИМЛ-измерений;
- системами для ИМЛ-измерений глюкозы могут быть портативные анализаторы глюкозы, госпитальные глюкометры (ИМЛ-глюкометры) и системы для непрерывного мониторинга глюкозы;
- контроль качества ИМЛ-измерений, как и лабораторных измерений, обеспечивается медицинским учреждением.
Несмотря на все удобство ИМЛ-измерений, существует ряд вопросов, связанных с использованием портативных глюкометров в медицинских организациях. Так как процедура забора образца капиллярной крови для дальнейшего анализа является инвазивной, и процесс нанесения капли крови на тест-полоску может быть сопряжен с контаминацией корпуса глюкометра, всегда присутствует риск передачи гемопатогенов через контаминированное оборудование или руки персонала. В том случае, если в медицинской организации индивидуальный глюкометр используется в качестве госпитального, то есть подразумевается его применение более чем у одного пациента, вероятность того, что такой глюкометр будет выступать в качестве фактора передачи гемоконтактных инфекций от пациента пациенту, несомненно, присутствует. Причем на каждые 100 новых пользователей глюкометра вероятность контаминации увеличивается на 6% (p = 0,0002) [2].
 Обеспечение качества и безопасности медицинской помощи – важнейшая стратегическая задача здравоохранения, неотъемлемой составляющей которой является обеспечение эпидемиологической безопасности пациентов и медицинского персонала [3]. Вопрос контроля гликемии в медицинских организациях объединяет в себе две глобальные проблемы – СД и необходимость постоянного контроля уровня глюкозы в крови со сложностью профилактики инфекций, связанных с оказанием медицинской помощи (ИСМП).
Обеспечение качества и безопасности медицинской помощи – важнейшая стратегическая задача здравоохранения, неотъемлемой составляющей которой является обеспечение эпидемиологической безопасности пациентов и медицинского персонала [3]. Вопрос контроля гликемии в медицинских организациях объединяет в себе две глобальные проблемы – СД и необходимость постоянного контроля уровня глюкозы в крови со сложностью профилактики инфекций, связанных с оказанием медицинской помощи (ИСМП).
В иностранной медицинской литературе приводятся данные, раскрывающие частоту контаминации глюкометров кровью в медицинских организациях [2], а также в других учреждениях, где может проводиться контроль гликемии при участии медицинского персонала [4]. Установлена роль контаминированного кровью оборудования для забора образца капиллярной крови и глюкометров во внутрибольничном распространении гепатита В от пациента пациенту [5–9].
R.F. Louie и соавт. [2] было проведено мультицентровое исследование, посвященное оценке частоты контаминации кровью глюкометров, используемых в условиях медицинских организаций. В исследовании приняли участие 12 больниц США. Для оценки были отобраны глюкометры, использующиеся для экспресс-диагностики у постели больного в ОРИТ, терапевтических, операционных и приемных отделениях, а также в поликлиниках. Среди исследуемых глюкометров были как электрохимические, так и фотометрические системы. Одни из них предполагали нанесение крови на тест-полоски, вставленные в прибор, то есть непосредственно при измерении – «on-meter» (n = 479), другие допускали нанесение крови на тест-полоски до их введения в глюкометр, то есть вне измерения – «off-meter» (n = 130) [2].
Пробы были отобраны с каждого участка, подлежащего исследованию (корпус глюкометра, гнездо для тест-полоски и место хранения). Образцы были проанализированы на наличие гемоглобина с помощью фенолфталеиновой пробы. Всего было исследовано 609 глюкометров, в том числе 116 из ОРИТ. Общий процент контаминированных глюкометров из разных медицинских организаций составил 30,2 ± 17,5 (от 0,0 до 60,5%). Доля контаминированных глюкометров, требующих нанесения крови на тест-полоску при измерении, составила 31,4 ± 19,1% (от 0,0 до 60,5%). Доля контаминированных глюкометров, предполагающих нанесение крови на тест-полоску до измерения, составила 26,6 ± 14,2% (от 10,2 до 35,5%) [2].
Средний процент контаминированных глюкометров в ОРИТ оказался равным 48,2 ± 30,2 (от 0,0 до 100,0%), в то время как в терапевтических отделениях – 26,9 ± 15,7 (от 0,0 до 58,8%). Среднее число контаминированных глюкометров в ОРИТ было в 2,2 раза выше, чем в терапевтических отделениях [2].
Наиболее подвержены контаминации кровью боковые поверхности глюкометров, кнопки управления и поверхности рядом с портом для тест-полоски. Важнейшие факторы контаминации окружающих предметов, рук пациентов и персонала – салфетки, с помощью которых стирают кровь с пальца перед измерением и после него, а также разбрызгивание мельчайших капель крови при извлечении использованной тест-полоски из порта глюкометра [10].
Место хранения глюкометров не учитывается как фактор риска контакта медработников с кровью и повторной контаминации обработанных глюкометров. Однако по данным R.F. Louie и соавт. [2], в среднем 20% участков для хранения глюкометров в 12 больницах были контаминированы, причем в некоторых медицинских центрах доля контаминации составила 52,7%. В ходе исследования было установлено, что нет единого понятия «место для хранения глюкометра», приборы могли находиться как на сестринском посту, так и в других помещениях.
Одно из возможных решений для предотвращения распространения гемоконтактных инфекций – выделение специального места для проведения ИМЛ, то есть оборудованной зоны в кабинете приема пациентов в условиях поликлиник и приемных отделений больниц; в условиях стационара контроль гликемии при участии медицинского персонала должен проводиться в процедурном кабинете. Если по ряду причин (тяжелое состояние пациента и т. д.) такая манипуляция проводится у постели больного, должны быть соблюдены санитарно-гигиенические правила: использование новой пары одноразовых перчаток при работе с каждым новым пациентом, дезинфекция глюкометра после каждого использования, утилизация тест-полосок как медицинских отходов, бывших в контакте с кровью пациента.
Несмотря на то что присутствие гемоглобина не указывает на наличие возбудителей гемоконтактных инфекций на поверхности глюкометра, оно предполагает такую возможность. При этом риску инфицирования подвержены как пациенты, так и персонал медицинских организаций [2].
Процесс внутрибольничного распространения гемоконтактных инфекций можно рассмотреть на примере гепатита В, вирус которого (ВГВ) может сохранять патогенность во внешней среде более 7 дней [11]. При этом инфицирующая доза составляет 0,0001 мкл сыворотки, содержащей ВГВ [12]. В США официально зарегистрированы случаи заражения гепатитами B и C, а также малярией через контаминированные медицинские приборы, в том числе через ручки для прокалывания, а также посредством глюкометров [9, 13].
Риск передачи гемоконтактных ИСМП особенно велик при исследованиях капиллярной крови, поскольку она с легкостью может попасть на руки персонала и на поверхности элементов измерительной системы. И, к сожалению, ИМЛ-измерения глюкозы занимают одно из первых мест по риску передачи гемоконтактных ИСМП [1].
Первое сообщение о передаче ИСМП при измерениях содержания глюкозы с помощью глюкометров было опубликовано в 1997 г. Центром по контролю заболеваемости США: почти одновременно произошли вспышки гепатита B у 9 пациентов в доме престарелых в Огайо и у 14 больных СД в одной из больниц Нью-Йорка. В обоих случаях средством передачи вируса послужили устройства для прокола кожи с одноразовыми стилетами, но с несменяемыми защитными колпачками (именно на них оставались следы крови) [1, 13]
В США с 1990 г. было расследовано не менее 18 внутрибольничных вспышек гепатита В. 15 (83%) из них были ассоциированы с недолжным использованием глюкометров или оборудованием для получения образца капиллярной крови. По меньшей мере 147 человек были инфицированы гепатитом В, в 4,1% случаев (6 человек) наблюдался летальный исход из-за развившихся осложнений острой формы инфекции. 140 (95%) человек из числа заболевших страдали СД [8]. Исследователи отмечают, что в США за последние 10 лет внутрибольничные вспышки гепатита В чаще регистрировались среди пациентов с СД, длительно находившихся в стационарах. Авторы отмечают также, что статистика, отражающая внутрибольничное распространение гепатита В, занижена [8], так как острая форма инфекции в 65% случаев протекает в безжелтушной форме, что затрудняет ее раннее выявление.
При расследовании вспышек было обнаружено, что в 12 (67%) случаях одноразовые ланцеты для прокола кожи использовались многократно. В остальных случаях не был использован новый колпачок для ланцета, либо использовался новый колпачок, хранившийся вместе со старыми (которые были контаминированы кровью). В 5 случаях использовались только одноразовые ланцеты, однако это не позволило исключить инфицирование, что говорит о наличии другого фактора, способствовавшего передаче инфекции. Дезинфекцию глюкометров перед использованием у разных пациентов не проводили ни в одном случае. При некоторых вспышках не соблюдались правила гигиены со стороны среднего медицинского персонала: медсестры не меняли перчатки перед осуществлением манипуляций у каждого пациента (или вовсе их не использовали) [8].
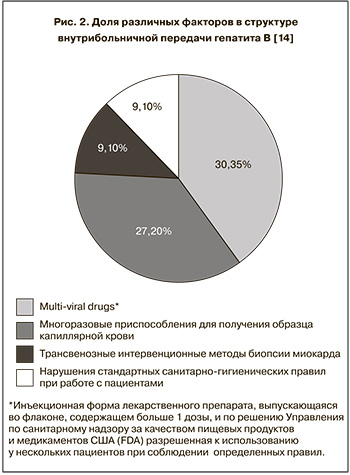
На рис. 1 представлено распределение внутрибольничных вспышек гепатита В по отделениям/учреждениям в США и странах Евросоюза в 1992–2007 гг., а на рис. 2 – обнаруженные факторы передачи гепатита В [14].
Процедуры, связанные с контролем гликемии, и нарушения гигиенических правил вместе составляют 36,3% факторов, приводящих к внутрибольничной передаче гемоконтактных инфекций, что подчеркивает их значимость и необходимость более пристального внимания к ним.
Роль вспомогательного оборудования для получения капли капиллярной крови в передаче ВГВ от пациента пациенту была установлена, в том числе, и с помощью молекулярно-генетического метода. В гематоонкологическом отделении одной из клиник Италии в период с 4 мая 2006 г. по 21 февраля 2007 г. среди пациентов было выявлено 3 новых случая ВГВ-инфекции. Генетическое типирование показало, что все случаи заражения были вызваны одним и тем же генетическим вариантом вируса. В ходе эпидемиологического расследования был установлен источник – пациент с хроническим гепатитом В. Обследование различных объектов внешней среды в отделении доказало роль «многопользовательского» (multi-patients) (но не многоразового!) ланцета, на котором был обнаружен ВГВ, генетически идентичный вызвавшему заболевание у других пациентов отделения [15].
О значимости проблемы безопасности медицинской помощи, включая профилактику ИСМП, свидетельствует то внимание, которое уделяется вопросам безопасности пациентов на международном и национальном уровнях [3]. При обеспечении безопасности медицинской помощи нет мелочей, поэтому внимание медицинского персонала должно быть приковано к любым деталям, представляющим для пациентов риск заражения ИСМП. В настоящее время поставлена глобальная задача по обеспечению безопасности пациентов: «чистая помощь – это более безопасная помощь», и все медицинские решения – от тактики лечения до оптимизации больничной среды – должны приниматься в интересах безопасности пациентов [3].
В связи с вышесказанным необходимо признать, что контаминация глюкометров кровью при отсутствии адекватной дезинфекции и должной обработки перед использованием у каждого пациента наравне с несоблюдением санитарно-гигиенических и противоэпидемических правил при их использовании и хранении являются факторами риска распространения гемоконтактных инфекций среди пациентов различных отделений клиник и учреждений, где производится контроль ГКК. К сожалению, в отечественной медицинской практике этому важному обстоятельству не уделялось должного внимания, и практически отсутствуют исследования, посвященные оценке распространенности и эпидемиологической значимости глюкометров как фактора передачи ИСМП.
На наш взгляд, также необходима разработка современных клинических рекомендаций по обеспечению эпидемиологической безопасности при определении уровня глюкозы в периферической крови и скорейшее внедрение их в практику.



