Опоясывающий лишай (ОЛ), или Herpes zoster, развивается вследствие реактивации латентного вируса Varicella zoster (VZV), сохранившегося в организме человека после первичного инфицирования, которое в большинстве случаев происходит в детском возрасте и протекает с клинической картиной ветряной оспы (ВО). После перенесенной острой инфекции вирус не элиминируется из организма, и наступает длительная латентная фаза [1–3].
Реактивация вируса происходит как при возрастном иммунодефиците [4], так и на фоне иммуносупрессии, возникшей вследствие сопутствующих заболеваний, в том числе ВИЧ-инфекции [5] и COVID-19 [6–8].
Учитывая, что более 95% людей старше 50 лет во всем мире ранее перенесли инфекцию VZV, большинство населения подвержено риску развития ОЛ [1, 9, 10].
Согласно опубликованным зарубежным данным, в странах Европы уровень заболеваемости колеблется от 2,0 до 4,6 на 1000 чел. [11], в США в течение жизни ОЛ заболевает почти каждый третий человек, и ежегодно в стране регистрируется до 1 млн новых случаев этого заболевания [12–14].
Сообщается, что в глобальном масштабе заболеваемость ОЛ растет, а в будущем это заболевание может перейти в ранг одного из наиболее широко распространенных инфекционных заболеваний среди взрослых [12]. В масштабном исследовании, проведенном в США с 1993 по 2016 г., включавшем 27 млн чел. старше 35 лет, расчетная заболеваемость ОЛ в 1993 г. составляла 2,5 на 1000 чел., в 2006 г. – 6,1, в 2016 г. – 7,2.[13–15]. Исследования, проведенные в Италии в 1999, 2004 и 2010 гг., также показали рост заболеваемости ОЛ с 1,59 до 6,31 на 1000 чел. в год [12].
Существует несколько гипотез, объясняющих неблагоприятные тенденции динамики заболеваемости ОЛ. Одной из них является гипотеза экзогенной бустерной иммунизации, согласно которой рост заболеваемости ОЛ связан с реализацией программ вакцинации детей против ВО, которые снижают вероятность контакта с VZV дикого типа и, соответственно, уменьшают вероятность естественного «бустер-эффекта» для перенесших в детстве острую инфекцию. Противоположная точка зрения заключается в том, что заболеваемость ОЛ росла еще до введения всеобщей вакцинации против ВО под влиянием демографических изменений и более широкого использования иммунодепрессантов [15].
Проведенные исследования доказали, что у лиц с иммунодефицитными состояниями риск возникновения ОЛ значительно выше. Так, у ВИЧ-инфицированных пациентов частота ОЛ в 8 раз превышает средний показатель заболеваемости лиц в возрасте от 20 до 50 лет, а среди пациентов отделений трансплантации органов и онкологических стационаров ОЛ заболевают до 25–50% больных с летальностью до 3–5% [2, 4, 16].
Заболеваемость ОЛ существенно различается при стратификации по возрасту. В систематическом обзоре, опубликованном в 2018 г., сообщалось, что в Северной Америке, Европе и Азиатско-Тихоокеанском регионе заболеваемость ОЛ в среднем составляет 3–5 случаев на 1000 чел. в год, среди населения в возрасте 60 лет – 6–8 случаев, в возрасте 80 лет – 8–12 случаев в год [12].
Поскольку во всем мире доля пожилых людей в популяции неуклонно растет, увеличивается и вероятность заболевания ОЛ, что неизбежно будет сопровождаться риском инвалидности и снижения качества жизни лиц зрелого возраста, при этом растет и экономический ущерб 12]. Так, в США только прямые медицинские расходы, связанные с ОЛ, составляют 2,6 млрд долларов в год [15].
В связи с высоким бременем ОЛ во многих странах мира одним из приоритетов здравоохранения является вакцинопрофилактика заболевания [10, 12]. Механизм действия вакцин против ОЛ заключается в повышении уровня иммунитета к VZV и подавлении реактивации вируса. В большинстве экономически развитых стран для профилактики ОЛ применяют вакцины двух основных видов – живую аттенуированную вакцину (в англоязычной литературе ZLV), разработанную Merck & Co. Inc., и адъювантную рекомбинантную субъединичную вакцину (RZV), разработанную GlaxoSmithKline, Inc. В Южной Корее используют инактивированную вакцину местного производителя, в Японии применяют ту же вакцину, которой прививают против ВО [15]. При этом в некоторых странах (Великобритания, Норвегия, Швеция) считают целесообразным одновременное внедрение в программы иммунизации всеобщей вакцинации детей против ВО и вакцинации пожилых лиц против ОЛ для предупреждения всплеска заболеваемости на фоне снижения циркуляции вируса дикого типа [17–19].
В Российской Федерации осуществляемый до недавнего времени эпидемиологический надзор за VZV-инфекцией предусматривал только статистическое наблюдение за заболеваемостью ВО и не включал эпидемиологический мониторинг ОЛ. Статистическая база по заболеваемости ОЛ начала формироваться только с 2019 г. Опубликованные в 2020 г. отечественные данные свидетельствовали, что в ряде субъектов Федерации в 2019 г. регистрировали высокую заболеваемость ОЛ с характерной территориальной неравномерностью распространения – преимущественно среди городского населения. Также были сделаны выводы, что самыми уязвимыми для ОЛ группами населения являлись лица пожилого возраста и пациенты с иммунодефицитными состояниями [20].
Цель исследования – эпидемиологическая характеристика ОЛ в Российской Федерации для обоснования мер по улучшению эпидемиологического надзора и профилактики этого заболевания в связи с актуальностью проблемы.
Материалы и методы
В работе использован эпидемиологический метод исследования, включая эпидемиологическое наблюдение, в рамках которого использовали описательно-оценочный и аналитический приемы.
Для оценки эпидемической ситуации изучены данные формы №2 Федерального государственного статистического наблюдения «Сведения об инфекционных и паразитарных заболеваниях» о заболеваемости ОЛ в Российской Федерации в возрастном разрезе и по субъектам РФ за 2019–2022 гг. Для более детальной оценки риска заболевания ОЛ в разных возрастных группах были изучены данные полицевой регистрации случаев ОЛ в системе АИС «ОРУИБ» отдела государственной регистрации инфекционных заболеваний ФБУЗ «Центр гигиены и эпидемиологии в городе Москве» за тот же период.
Для оценки взаимосвязи между уровнями заболеваемости ОЛ в субъектах РФ и впервые выявленными случаями болезни, вызванной ВИЧ, а также бессимптомным инфекционным статусом, вызванным ВИЧ, статистическому анализу были подвергнуты также интенсивные показатели заболеваемости болезнью, вызванной ВИЧ, и носительства ВИЧ (2019–2022 гг.). Особенности связи между заболеваемостью ОЛ и ВИЧ изучены методом корреляции (метод квадратов Пирсона). Были определены сила этой связи и направление, а также оценена достоверность коэффициента корреляции (r).
Для оценки экономической значимости ОЛ в РФ была использована рассчитанная нами ранее «стандартная» величина экономического ущерба, наносимого одним случаем данного заболевания [21], проиндексированная с учетом уровня инфляции по данным Росстата. Величину ежегодного ущерба от ОЛ определяли путем умножения «стандартной» величины экономического ущерба от 1 случая заболевания на число случаев, зарегистрированных в данном году.
Результаты
По данным формы № 2 за 2019–2022 гг., в РФ ежегодно регистрировали от 13,5 до 19,5 тыс. случаев ОЛ. Показатели заболеваемости ОЛ среди совокупного населения находились на уровне 9,2–13,1 на 100 тыс. населения.
В 2020–2021 гг. на фоне высокой заболеваемости населения новой коронавирусной инфекцией COVID- 19 среднероссийские показатели заболеваемости ОЛ находились на более низком уровне, чем в 2019 г. (10,3 и 9,2 на 100 тыс. против 13,1 в 2019 г.). Вместе с тем в 2020–2021 гг. было зарегистрировано более 80% всех случаев ОЛ с летальными исходами за весь период статистического наблюдения.
Эпидемиологический анализ показал, что бремя ОЛ существенно различается в субъектах РФ. В 2022 г. более чем в 20 субъектах показатели превышали средний по стране уровень заболеваемости в 2–3 раза. Наиболее высокие показатели заболеваемости ОЛ в 2022 г. были зарегистрированы в г. Севастополе (60,8 на 100 тыс. населения, что в 5,5 раза выше среднероссийского показателя), в Иркутской (37,5 на 100 тыс.), Челябинской (37,3), Курской (35,6), Смоленской (35,5) и Кемеровской (33,0) областях, что в 3–3,5 раза превышает среднероссийский показатель (рис. 1).
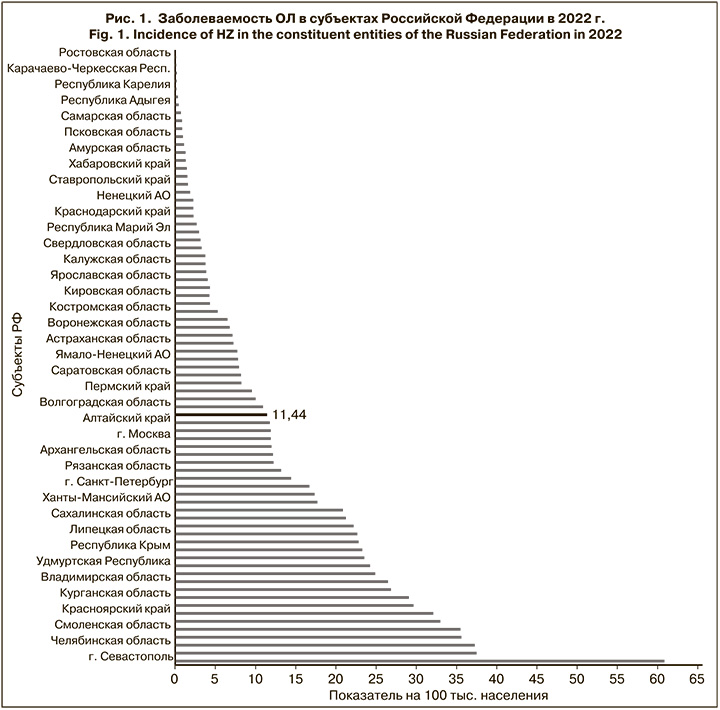
Аналогичная ситуация наблюдалась в 2019–2021 гг. Вместе с тем с 2019 г. случаи ОЛ не регистрировались в республиках Калмыкия, Дагестан, Северная Осетия, Тыва, Чеченской Республике, Еврейской автономной области.
Для установления причин выявленных различий заболеваемости ОЛ в субъектах РФ в рамках настоящего исследования был проведен корреляционный анализ между показателями заболеваемости впервые выявленной болезнью, вызванной ВИЧ, бессимптомным инфекционным статусом, вызванным ВИЧ, и показателями заболеваемости ОЛ в субъектах Российской Федерации в 2019–2022 гг.
Статистическая обработка полученных результатов показала, что между исследуемыми показателями в 2020, 2021 и 2022 гг. существовала прямая умеренной силы корреляционная связь: коэффициенты корреляции составили +0,41 ± 0,09; +0,37 ± 0,09 и +0,38 ± 0,09 соответственно (р < 0,01) (табл. 1).
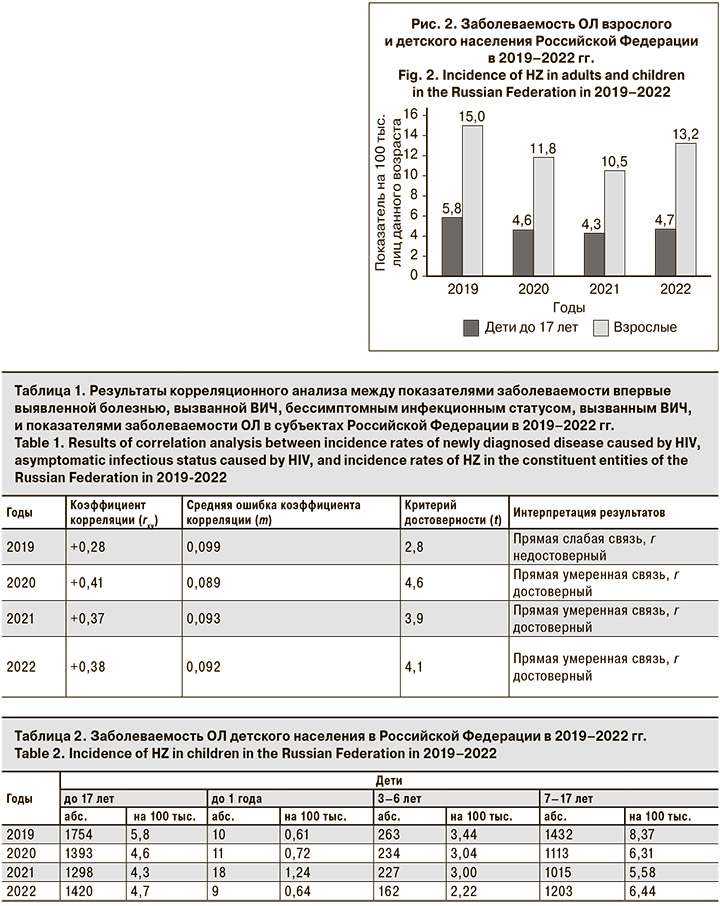
Анализ заболеваемости ОЛ по возрастным группам позволил установить, что в целом в РФ в возрастной структуре заболевших ежегодно более 90% составляли взрослые, и показатели заболеваемости среди них в 2,5 раза превышали показатели детской заболеваемости (рис. 2).
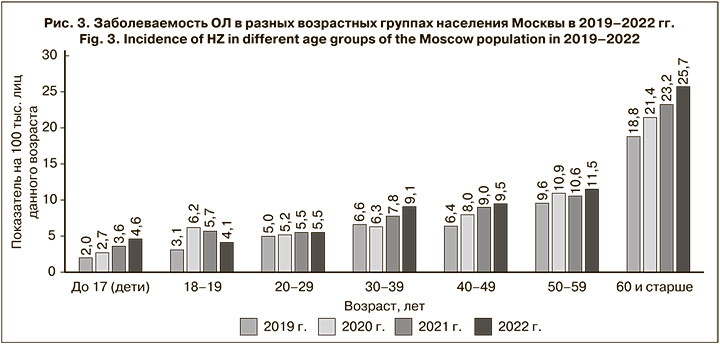
Анализ заболеваемости ОЛ населения Москвы показал, что ОЛ регистрируют во всех возрастных группах, при этом с возрастом показатели заболеваемости увеличиваются. Среднемноголетний уровень заболеваемости взрослых в Москве составлял 10–12 на 100 тыс., среди лиц в возрасте до 29 лет – около 5 на 100 тыс., 30–39 и 40–49 лет – 6–9, 50–50 лет – 10–11, старше 60 лет – 19–25 на 100 тыс. населения данного возраста (рис. 3).
Среди детского населения в РФ ежегодно диагностировали 1298–1754 случаев ОЛ. Уровни заболеваемости детей до 17 лет составляли 4,3–5,8 на 100 тыс. детей (см. рис. 2; табл. 2).
Наиболее высокие показатели заболеваемости ОЛ отмечены у детей школьного возраста. При этом случаи заболевания регистрировали и у детей младенческого возраста (до 1 года).
По ориентировочным расчетам, проведенным в 2022 г., прямые и непрямые экономические потери от 1 случая ОЛ составляли около 144 тыс. руб., а ущерб от всех зарегистрированных случаев – почти 2,5 млрд руб.
Обсуждение
Впервые полученные в РФ статистические данные о заболеваемости населения ОЛ (за период 2019–2022 гг.) существенно отличаются от таковых в странах Европы, Азиатско-Тихоокеанского региона и Северной Америки: в РФ ежегодные уровни заболеваемости ОЛ были в 30–50 раз ниже, чем в других странах: 9,2–13,1 на 100 тыс. населения в год в РФ против 3–5 случаев на 1000 чел. в год в среднем в других странах [11, 12).
Во время эпидемии COVID-19 в 2020 г. среди совокупного населения РФ показатели заболеваемости ОЛ снизились, а к 2022 г. приблизились к уровню 2019 г. Вместе с тем данные о зарегистрированных летальных исходах ОЛ в этот период могут свидетельствовать о более тяжелом течении заболевания на фоне CОVID- 19.
Значительная разница в уровнях заболеваемости ОЛ в субъектах РФ, а также в России по сравнению с другими странами позволяет предположить, что на начальном этапе внедрения эпидемиологического надзора за ОЛ в РФ медицинскими организациями осуществляется неполная регистрация случаев заболевания.
На уровень заболеваемости ОЛ может влиять целый ряд факторов.
Так, в публикациях ВОЗ сообщалось, что ОЛ может быть значительной проблемой для регионов с высоким уровнем заболеваемости ВИЧ-инфекцией [9].
Проведенный в ходе данного исследования корреляционный анализ между показателями заболеваемости впервые выявленной болезнью, вызванной ВИЧ, бессимптомным инфекционным статусом, вызванным ВИЧ, и показателями заболеваемости ОЛ в субъектах Российской Федерации выявил прямую связь между этими величинами (в 2020–2022 гг. r составил +0,41 ± 0,09; +0,37 ± 0,09 и +0,38 ± 0,09 соответственно; р < 0,01).
Согласно результатам исследования, лица молодого трудоспособного возраста (до 49 лет) в структуре заболевших ежегодно составляли около 30%.
При этом у лиц молодого возраста, живущих с ВИЧ, ОЛ встречается чаще, чем среди населения в целом, и, несмотря на молодой возраст, частота осложнений этого заболевания у больных ВИЧ-инфекцией высока. Кроме того, данная категория больных подвержена более высокому риску развития тяжелых форм генерализованной инфекции и рецидивирующего течения ОЛ, требующих длительного стационарного лечения [2, 16].
Учитывая, что ОЛ является ранним маркером приобретенного иммунодефицита при естественном течении ВИЧ-инфекции, и нередко это заболевание развивается за несколько лет до появления других оппортунистических инфекций и указывает на нарастающую иммуносупрессию [16], специалистам здравоохранения необходимо знать, что ОЛ может являться первым клиническим признаком ВИЧ-инфекции.
Помимо косвенного указания на болезнь, вызванную ВИЧ, ОЛ может являться признаком иммунодефицитного состояния другого генеза. Так, авторы из Таджикистана [22] опубликовали данные, что по результатам полноценного онкопоиска, проведенного у 15 больных тяжелым ОЛ, у 9 (60%) были диагностированы онкологические заболевания.
Оказывать влияние на уровни заболеваемости ОЛ на территориях могут и демографические показатели, а именно доля пожилых людей в общей численности населения субъектов РФ.
Результаты проведенного исследования подтвердили зарубежные данные о том, что среди лиц в возрасте 60 лет и старше интенсивные показатели заболеваемости ОЛ значительно выше, чем в других возрастных группах [12, 15].
Как показали полученные результаты, проблема заболеваемости ОЛ актуальна и для педиатрии. Надзор за ОЛ среди детского населения особенно важен в условиях отсутствия в Российской Федерации национальной программы иммунизации детей против ВО, так как заболевшие ОЛ являются источниками возбудителя инфекции для неиммунных детей.
Ежегодно около 10% всех случаев заболевания ОЛ (более 1300 случаев) приходилось на детей разных возрастных групп, в том числе младенческого возраста (до 1 года).
Имеются данные о том, что у некоторых детей и подростков диагностируют ОЛ без ВО в анамнезе. Это объясняется транзиторным снижением активности клеточных реакций в результате стрессов после предшествующих эпизодов бессимптомной вирусной инфекции [1]. Также доказана возможность развития ОЛ и у детей первых лет жизни в результате приобретения новорожденным VZV-латентной инфекции от матери, заражение которой произошло во второй половине беременности [23, 24]. В связи с этим факты заболевания ОЛ детей первого года жизни в РФ настораживают и требуют изучения, так как могут свидетельствовать о перенесенной внутриутробно VZV-инфекции.
Высокая заболеваемость ОЛ во многих странах мира влечет значительные социальные и экономические издержки [2, 15].
На основе оценки распространенности ОЛ в разных возрастных группах населения РФ, опираясь на мировые и отечественные данные о частоте осложнений и длительности лечения этого заболевания, а также учитывая стандарты диагностики и лечения ОЛ, стоимость лекарственных препаратов и величину ВВП в РФ, нами был проведен расчет экономического ущерба от этого заболевания.
Полученные ориентировочные данные об экономическом ущербе от всех зарегистрированных случаев ОЛ (2,5 млрд руб. в год) также свидетельствуют о значимости для экономики РФ рецидивирующей формы инфекции Varicella zoster, а в условиях полной статистической регистрации случаев ОЛ ущерб для экономики страны от заболеваемости ОЛ может оказаться еще выше.
Заключение
ОЛ является существенной проблемой для общественного здравоохранения и экономики страны. Случаи заболевания этой формой VZV-инфекции в РФ встречаются во всех возрастных группах – с первых месяцев жизни до пожилого возраста с максимальными показателями среди лиц в возрасте старше 60 лет регистрируются летальные исходы. С увеличением продолжительности жизни населения страны, а также ростом в популяции доли лиц с иммунодефицитными заболеваниями и появлением новых показаний к иммуносупрессивной терапии заболеваемость ОЛ может возрасти.
В отсутствие плановой вакцинопрофилактики ВО высокая заболеваемость населения ОЛ существенно повышает риски заражения ВО для восприимчивых людей.
К сожалению, проводимые в настоящее время профилактические мероприятия в отношении ОЛ неспецифичны, сводятся в основном к пропаганде здорового образа жизни и, следовательно, не могут оказать существенного влияния на уровень заболеваемости.
Для уменьшения бремени ОЛ в стране требуется внедрение более эффективных мер профилактики, в том числе проведение плановой иммунизации лиц пожилого возраста и пациентов с иммунодефицитными состояниями, для чего требуется разработка отечественных вакцинных препаратов для профилактики ОЛ.
Для своевременного прогнозирования эпидемической ситуации и оптимизации тактики профилактики необходимо усиление эпидемиологического надзора за инфекцией, вызванной вирусом Varicella zoster, в том числе за ОЛ, в соответствии с Методическими рекомендациями «Эпидемиологический надзор за инфекцией, вызываемой вирусом Varicella zoster», утвержденными Главным государственным санитарным врачом РФ 14.12.2020.



